Microdigest 3
CTAD : ce qu’il faut retenir
Découvrez un résumé des principales données présentées lors de la conférence CTAD 2024 en ce qui concerne les nouveaux biomarqueurs et les traitements anti-amyloïdes.

Sélection dans le cadre des essais cliniques
Messages clés:
- Le ratio de p-tau 217 est un biomarqueur qui permet de réduire les taux d’échec du dépistage via la tomographie par émission de positons (TEP) des plaques amyloïdes, quelles que soient les origines ethniques des patients.
- Les taux inférieurs d’éligibilité dans le cadre des analyses plasmatiques indiquent que les niveaux anormaux d’amyloïde sont moins prévalents parmi les minorités ethniques, si bien que ces groupes sont mal représentés dans les essais portant sur les anti-amyloïdes.
- Les niveaux de protéine tau à la TEP sont un critère d’évaluation pertinent qui présente une corrélation élevée avec la fonction cognitive.
Étude AHEAD 3-45 : méthodologie et résultats d’un nouveau processus de sélection pour un essai préclinique portant sur la MA (Résumé : LBS1)
L’étude AHEAD 3-45 se compose de deux volets :
- A3 est un essai de phase 2, d’une durée de 4 ans, portant sur le lécanemab intraveineux (titration de 5 mg/kg suivie de 10 mg/kg par mois pendant 208 semaines) par rapport à un placebo chez des personnes ne présentant pas de troubles cognitifs et dont la TEP à l’amyloïde-β est intermédiaire (20-40 centiloïdes [CL]). L’objectif est de prévenir le déclin cognitif (Preclinical Alzheimer’s Cognitive Composite 5 [PACC-5]) sur une période de 4 ans.
- A45 est un essai de phase 3, d’une durée de 4 ans, portant sur le lécanemab intraveineux (5 mg/kg toutes les deux semaines pendant 6 semaines, puis 10 mg/kg toutes les deux semaines pendant 86 semaines, puis tous les mois pendant 120 semaines) par rapport à un placebo chez des personnes ne présentant pas de troubles cognitifs et positives à la TEP à l’amyloïde-β (≥40 CL). L’objectif est de ralentir l’accumulation de l’amyloïde-β (TEP amyloïde et TEP tau).
La période de sélection vient de s’achever.
Screening des biomarqueurs plasmatiques, de l’amyloïde et de l’imagerie TEP tau dans l’étude AHEAD 3-45 (Présentation 2)
Présentateur : Reisa Sperling (États-Unis)
- Processus d’examen préalable pour l’A3 et l’A45 :
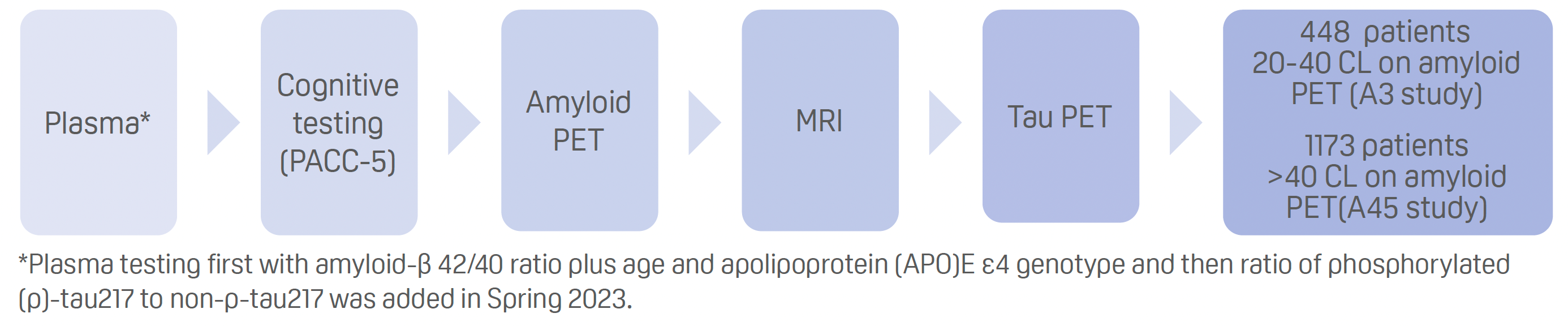
Résultats:
- L’inclusion d’un test plasmatique pour le rapport amyloïde-β42/40 a réduit le taux d’échec de la TEP amyloïde pour prédire plus de 11 CL d’environ 75 % à environ 55 %.
- L’ajout du rapport p-tau217 a encore réduit le taux d’échec de la TEP amyloïde pour prédire plus de 18 CL à environ 40-45%.
- Le rapport p-tau217 plasmatique a atteint une aire sous la courbe caractéristique opérationnelle du récepteur de 0,95 pour la TEP amyloïde sur 20 CL d’éligibilité.
- L’analyse du plasma avec le modèle complet d’analyse du plasma a permis de réduire à 25 % le taux d’échec de la TEP amyloïde pour la prédiction de plus de 40 CL.
- La TEP tau du lobe temporal médian et du néocortex était plus élevée chez les participants de l’étude A45 que chez ceux de l’étude A3.
- La TEP Tau a montré la corrélation la plus forte avec la cognition sur le PACC-5.
“L‘augmentation précoce du rapport p-tau217 peut s’avérer utile pour des essais interventionnels encore plus précoces visant à prévenir la positivité future de l’amyloïde”, a déclaré Sperling. “Les résultats confirment que la TEP à la protéine tau est un critère d’évaluation clé, servant de passerelle potentielle entre l’imagerie, les biomarqueurs et la cognition entre A3 et A45.”
Différences raciales et ethniques dans les taux d’éligibilité des biomarqueurs plasmatiques p-tau217 dans un essai préclinique sur la MA (Présentation 3)
Présentateur : Doris Molina Henry
- Comprendre la capacité de l’algorithme des biomarqueurs plasmatiques, pendant la fenêtre où le rapport p-tau 217 a été ajouté, à détecter l’éligibilité à la TEP amyloïde à plus de 18 CL dans différents groupes raciaux et ethniques sous-représentés.
Résultats:
- Des taux d’éligibilité au plasma inférieurs dans tous les groupes raciaux et ethniques sous-représentés par rapport aux adultes blancs non hispaniques.
- Les taux d’éligibilité à la TEP parmi les participants éligibles au plasma étaient comparables pour les différents groupes raciaux/ethniques, sans différence significative.
| Racial/ethnic group | Number | Plasma eligibility rate | % of plasma eligible patients who were also PET eligible |
|---|---|---|---|
| Non-Hispanic Asian | 155 | 15% | 50% |
| Hispanic White | 877 | 19% | 63% |
| Non-Hispanic Black | 511 | 19% | 68% |
| Non-Hispanic White | 4832 | 27% | 71% |
| Hispanic Black | 62 | 11% | 75% |
“Les taux plus faibles d’éligibilité du plasma suggèrent une prévalence différentielle de l’anomalie amyloïde dans ces groupes […], ce qui laisse supposer que les niveaux d’amyloïde sont plus faibles chez les individus issus de groupes sous-représentés sur le plan racial et ethnique, ce qui contribue à leur sous-représentation dans les essais anti-amyloïde”, a déclaré Henry.
“L‘éligibilité à la TEP était la même dans tous les groupes, ce qui prouve que les mêmes algorithmes de prédiction du plasma ont été appliqués de manière appropriée dans tous les groupes raciaux et ethniques”, a-t-elle ajouté.
“Cela suggère […] que d’autres facteurs peuvent expliquer le risque plus élevé de démence chez les personnes appartenant à des groupes raciaux et ethniques sous-représentés qui ont une prévalence plus faible de l’amyloïde.
Biomarqueurs et diagnostic de la maladie d’Alzheimer
Principaux enseignements:
- La β-synucléine pourrait représenter un nouveau biomarqueur synaptique sanguin dans la maladie d’Alzheimer.
- Le temps passé à chaque unité de 0,5 de l’échelle d’évaluation de la démence clinique (Clinical Dementia Rating Scale-Sum of Boxes) pourrait aider à évaluer la réponse au traitement.
- Un test de biomarqueurs sanguins multi-analytes peut faciliter la prise de décision en matière de diagnostic.
- Les disparités raciales/ethniques dans la positivité de la tomographie par émission de positons (TEP) de l’amyloïde et dans le stade clinique au moment du diagnostic doivent être corrigées pour améliorer l’accès au traitement.
- Des stratégies doivent être développées pour faciliter l’interprétation des performances de p-tau217 dans le contexte de conditions médicales comorbides telles que l’insuffisance rénale chronique.
- Les différents rôles des biomarqueurs sanguins pourraient ouvrir la voie à une approche diagnostique progressive de la maladie d’Alzheimer.
- Des tests supplémentaires sont recommandés lorsque le liquide céphalorachidien (LCR) et les mesures TEP diffèrent quant à la positivité de l’amyloïde-β avant de recommander un traitement anti-amyloïde.
Augmentation précoce du marqueur sanguin synaptique β-synucléine chez les individus asymptomatiques atteints de la maladie d’Alzheimer autosomique dominante (Abstract ID OC14) la maladie d’Alzheimer autosomique dominante (Abstract ID OC14)
Présentateur : Patrick Oeckl (Allemagne)
- La spectrométrie de masse par immunoprécipitation a été utilisée pour quantifier la protéine pré-synaptique β-synucléine dans les échantillons de sang de 178 participants à l’étude DIAN (Dominantly Inherited Alzheimer Network).
- Ont été inclus 31 porteurs de mutations symptomatiques, 78 porteurs de mutations asymptomatiques et 69 non porteurs de mutations sans troubles cognitifs.
Résultats:
- Les taux de β-synucléine étaient significativement plus élevés chez les patients asymptomatiques atteints de la maladie d’Alzheimer autosomique que chez les personnes sans troubles cognitifs, et plus élevés chez les patients symptomatiques.
- Les taux sanguins de β-synucléine ont commencé à augmenter chez les porteurs de la mutation environ 11 ans avant l’apparition des symptômes.
- Classement selon le moment où les niveaux de biomarqueurs liquides divergent de manière significative entre les porteurs et les non-porteurs de mutation, du plus précoce au plus tardif :
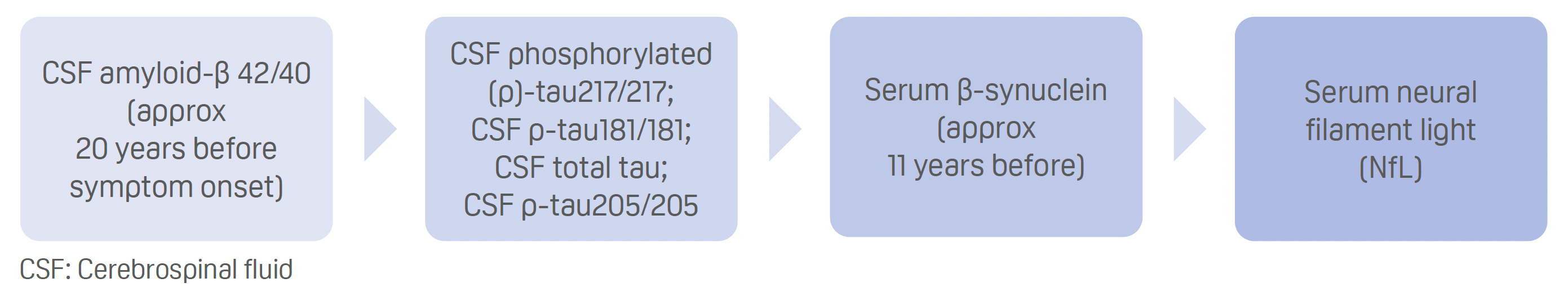
- La trajectoire de la β-synucléine sérique précède les mesures d’imagerie de la déficience cognitive, de l’atrophie cérébrale et de l’hypométabolisme.
- La β-synucléine sérique avait une capacité modérée à prédire la positivité de l’amyloïde-β (aire sous la courbe caractéristique d’exploitation du récepteur de 0,75).
- La β-synucléine sérique présente une corrélation significative avec les troubles cognitifs.
La β-synucléine sanguine pourrait être un “marqueur synaptique facilement accessible pour le diagnostic, le pronostic, [and] le développement de médicaments”, a déclaré Oeckl.
Progression clinique sur le CDR-SB : temps de séjour à chaque niveau dans les cohortes DIAN et ADNI (Abstract OC19)
Présentateur : Guoqiao Wang (USA)
- Le temps que les personnes passent à chaque unité de 0,5 de l’échelle d’évaluation de la démence clinique – somme des cases (CDR- SB) avant de passer au niveau suivant, appelé temps de résidence, a été examiné dans deux cohortes – DIAN (MA autosomique dominante) et ADNI (MA sporadique) en utilisant un modèle d’effets aléatoires pour la progression de la maladie.
Résultats:
- Maladie d’Alzheimer à dominance autosomique : Durée de séjour par 0,5 unité CDR-SB de 0,5 an ou moins lorsque le CDR-SB atteint 3 points ou plus.
- AD sporadique : Durée de séjour par 0,5 unité CDR-SB de 0,5 an ou moins lorsque le CDR-SB atteint 3,5 points ou plus.
- Temps de séjour pour passer d’un score CDR-SB de 0,5 à 3,5 points : 6,5 ans en moyenne pour la MA autosomique dominante et 5,6 ans pour la MA sporadique, soit une différence d’environ 0,9 an.
En utilisant le temps de résidence, un effet de traitement pourrait être calculé pour les patients de la phase d’extension ouverte de l’essai Clarity AD sur le lecanemab, par exemple :
- À partir d’un score CDR-SB de base de 3,17 points, il a été estimé que les patients traités par placebo mettraient 2,3 ans à diminuer de 3,09 points et que ceux traités par lecanemab mettraient 3,0 ans, soit un retard de 0,7 an dans la progression de la maladie.
Le temps de séjour à chaque niveau de 0,5 unité dans le CDR-SB “pourrait fournir une méthode alternative standardisée pour interpréter et évaluer l’effet du traitement“, a déclaré Wang.
Divergences entre les déterminations de l’amyloïde cérébrale élevée dans le LCR et la TEP et leur signification pronostique (Résumé : LB10)
Présentateur : David Knopman (USA)
- Le déclin cognitif consécutif à des mesures discordantes de la positivité de l’amyloïde-β dans le LCR et la TEP a été évalué chez 587 participants de la cohorte ADNI souffrant de troubles cognitifs légers.
Résultats:
- Les résultats discordants étaient peu fréquents, avec un taux d’environ 5 %.
- Les patients ayant obtenu des résultats négatifs pour l’amyloïde dans le LCR et la TEP et ceux ayant obtenu des résultats discordants (négatifs pour l’un ou l’autre des tests) présentaient une cognition similaire au départ, et la cognition était meilleure par rapport aux patients ayant obtenu des résultats positifs pour les deux mesures.
- Chez les patients positifs à l’amyloïde dans le LCR mais pas à l’amyloïde dans la TEP, les rapports p-tau/amyloïde-β dans le LCR étaient nettement inférieurs à ceux des patients positifs aux deux mesures.
- Sur une période médiane de 4 ans de suivi, les patients dont les résultats étaient discordants n’ont pas présenté de baisse significative des scores au Rey auditory Verbal Learning Test Sum of Trials 1-6 ou au Clinical Dementia Rating Scale-Sum of Boxes, contrairement aux patients dont les tests étaient positifs pour ces deux mesures.
- Les taux de démence incidente au cours du suivi n’étaient significativement élevés que chez les patients dont le test était positif pour les deux mesures (17,3 pour 100 personnes-années), tandis que les patients dont le test était négatif ou dont les résultats étaient discordants pour les deux mesures présentaient des taux similaires (allant de 1,9 à 3,0 pour 100 personnes-années).
“Étant donné que les personnes dont le LCR est positif et la TEP négative n’ont pas présenté de déclin au sein du groupe, il convient d’obtenir des preuves supplémentaires de la probabilité de progression de la maladie avant de recommander un traitement par anticorps monoclonal anti-amyloïde”, a déclaré le Dr Knopman.
Évaluation de l’impact d’un test de biomarqueurs sanguins multi-analytes pour l’évaluation des troubles cognitifs : résultats de l’étude d’utilité clinique QUIP II (Abstract OC32)
Présentateur : Joel Braunstein (USA)
- Douze cliniciens traitant 203 patients atteints de troubles cognitifs ont été interrogés pour évaluer l’utilisation de PrecivityAD2 (C2N Diagnostics, St Louis, Missouri, États-Unis) dans la gestion clinique et la prise de décision.
- Le test sanguin quantifie les niveaux plasmatiques d’amyloïde-β42 et 40 ainsi que de p-tau217 et de non-p-tau217 pour donner un score de probabilité amyloïde (APS)2, de 0 à 100 points, où un score de 0 à 47 signifie un résultat négatif et une faible probabilité de positivité de l’amyloïde et un score de 48 à 100 points un résultat positif et une forte probabilité.
Résultats :
- 51% des patients ont été testés négatifs.
- 99 % de conformité avec l’utilisation prévue.
- 75 % de changement dans la certitude diagnostique de la maladie d’Alzheimer, dans le traitement médicamenteux ou dans les évaluations ultérieures de l’amyloïde cérébrale.
- Faible corrélation entre le résultat de l’APS2 et la probabilité de maladie d’Alzheimer rapportée par le clinicien avant l’utilisation du test sanguin, et forte corrélation après l’utilisation du test sanguin.
- Pour les patients négatifs, la probabilité de MA rapportée par le clinicien a diminué de 53 % avant l’utilisation du test sanguin à 11 %, et pour les patients positifs, elle a augmenté de 65 % à 93 %.
- On a constaté une diminution significative de la prescription de médicaments contre la MA chez les patients négatifs avant et après l’utilisation du test sanguin et une augmentation significative chez les patients positifs.
- Les tests supplémentaires d’amyloïde cérébrale ont diminué de 70 % chez les patients négatifs et de 26 % chez les patients positifs.
“Nous pensons […] que le test sanguin PrecivityAD2™ a conduit à des changements cliniquement significatifs dans la prise de décision concernant la certitude diagnostique de la MA, la gestion du traitement médicamenteux et l’évaluation supplémentaire de l’amyloïde chez les patients évalués pour des troubles cognitifs”, a déclaré Braunstein.
Présentateur : Gil Rabinovici (USA)
Différences entre les résultats de la TEP à l’amyloïde et les déterminants sociaux de la santé en fonction de la race ou de l’origine ethnique : résultats de New IDEAS (Résumé OC08)
- Les taux de positivité de la TEP amyloïde, le stade clinique et les déterminants sociaux de la santé ont été comparés chez 4 845 participants à l’étude New IDEAS atteints de troubles cognitifs légers (MCI ; 64 %) ou de démence (37 %), dont 21 % se sont déclarés noirs/africains américains (BAA), 18 % latinos/hispaniques (LAT) et 61 % d’une autre race ou d’une autre ethnie (NBL).
Résultats
Les groupes BAA et LA étaient les suivants
- une probabilité significativement inférieure de 28 % à celle du groupe NBL d’être positif à la TEP amyloïde, avec des taux respectifs de 60,7 % et 60,8 % par rapport à 68,2 % ;
- plus susceptibles de présenter des comorbidités vasculaires, telles que l’hypertension (73,3 et 61,5 vs 54,3 %) et le diabète (29,9 % et 29,8 % vs 16,3 %) ;
- plus susceptibles de présenter une démence, par rapport au DCL, que le groupe NBL, avec un taux de 47,4 % et 43,5 % contre 30,5 % ;
- plus susceptibles d’avoir une présentation atypique et donc plus difficiles à diagnostiquer (36,0 % et 35,55 contre 26,6 %) ;
- plus susceptibles d’avoir des scores moyens au mini-examen de l’état mental plus faibles au départ que le groupe LNB (21 et 21 vs 25 points).
“Il est essentiel de s’attaquer à ces disparités modifiables pour améliorer l’équité dans l’accès aux soins et la mise en œuvre des stratégies de prévention de la démence”, a déclaré M. Rabinovici.
Performance du plasma p-tau217 dans une cohorte afro-américaine : résultats de l’étude African Americans fighting Alzheimer’s in midlife study (Résumé : OC13)
Présentateur : Gilda Ennis (USA)
- La précision du p-tau217 plasmatique pour détecter la positivité de la TEP amyloïde a été évaluée chez 233 adultes sans troubles cognitifs identifiés comme noirs ou afro-américains non hispaniques de la cohorte AA-FAIM et présentant au moins l’une des comorbidités suivantes : altération de la fonction rénale, maladie cardiovasculaire, hypertension artérielle, diabète ou obésité.
Résultats
- Des niveaux plus élevés de p-tau217 dans le plasma ont été significativement associés à une insuffisance rénale légère (débit de filtration glomérulaire estimé [eGFR] inférieur à 90 ml/min par 1,73m2) et modérée à sévère (DFGe inférieur à 60 ml/min par 1,73m2), ainsi qu’à une maladie cardiovasculaire (infarctus du myocarde, accident vasculaire cérébral ou insuffisance cardiaque congestive).
- Aucune des deux associations n’a pu être expliquée par la charge amyloïde dans de petits sous-échantillons de 38 et 64 individus, respectivement.
- Les taux plasmatiques de p-tau217 n’étaient pas significativement plus élevés chez les patients souffrant d’hypertension de stade 1 ou 2, de diabète ou d’obésité, après prise en compte de l’âge et du sexe.
- La précision du p-tau217 plasmatique pour détecter la positivité de la TEP amyloïde chez 65 patients de la cohorte AA-FAIM était de 90 % à un seuil de 0,35 pg/mL, avec une sensibilité de 94 % et une spécificité de 80 % (l’initiative Global CEO sur la MA recommande 90 % et 85 %, respectivement, pour l’utilisation de biomarqueurs sanguins dans les soins primaires).
“Nous devons étudier des stratégies pour faciliter l’interprétation précise de la p-tau 217 plasmatique dans le contexte de conditions médicales qui augmentent ou diminuent faussement la p-tau 217″, a déclaré Ennis.
Rôles différentiels des biomarqueurs plasmatiques de la maladie d’Alzheimer dans le cadre d’un diagnostic par étapes guidé par des biomarqueurs : comparaison directe au sein d’une population asiatique (Résumé : OC38)
Présentateur : Daeun Shin (République de Corée)
- Les rôles différentiels des marqueurs plasmatiques ont été étudiés chez 2984 Asiatiques (22% sans troubles cognitifs, 68% avec troubles cognitifs de la MA, 6% avec troubles cognitifs vasculaires sous-corticaux, 3% avec démence frontotemporale) pour voir s’ils pouvaient être utilisés dans le cadre d’une stratégie par étapes pour un diagnostic plus efficace de la MA guidé par les biomarqueurs.
- Biomarqueurs plasmatiques étudiés : amyloïde-β 42/40 ; p-tau181 ; p-tau217 ; p-tau231 ; GFAP ; NfL.
Résultats
| Best biomarker | Role | AUC |
|---|---|---|
| Nfl | Distinguished patients with any cognitive impairment from unimpaired individuals | 0.71–0.94 |
| p-tau217 | Discriminated amyloid-β PET positivity in all groups | 0.88–0.95 |
| p-tau217 | Discriminated tau PET positivity in AD cognitively impaired patients | 0.90–0.91 |
| p-tau217 | Distinguished amyloid-β PET-positive patients with AD cognitive impairment from amyloid-β PET-negative patients with non-AD dementias. | 0.94–0.95 |
| p-tau217 and then GFAP | Predicted cognitive decline in cognitively unimpaired patients | N/A |
AUC : aire sous la courbe caractéristique du récepteur ; N/A ; non applicable ; NfL ; neurofilament light ; p : phosphorylé ; PET : tomographie par émission de positrons ; GFAP : protéine acide fibrillaire gliale.
“Ces résultats soulignent l’importance des rôles différentiels des biomarqueurs plasmatiques de la maladie d’Alzheimer dans une approche diagnostique progressive”, a déclaré M. Shin. a déclaré M. Shin.
Thérapies anti-amyloïdes
Principaux enseignements:
- Des recommandations d’utilisation appropriées ont été émises pour le donanemab afin d’aider à identifier les candidats appropriés au traitement.
- L’éligibilité au traitement anti-amyloïde est relativement faible et pourrait être améliorée par un dépistage plus large incluant des biomarqueurs sanguins.
- Les patients en situation réelle sont sélectionnés de manière appropriée et reçoivent le lécanemab conformément aux informations d’étiquetage approuvées par la FDA.
- Lecanemab est bien toléré par les patients en clinique et les taux d’observance sont bons.
Donanemab : recommandations sur l’utilisation appropriée (Abstract : LB01))
Présentateur : Gil Rabinovici (USA)
- Les recommandations ont été élaborées par le groupe de travail thérapeutique sur la maladie d’Alzheimer et les troubles apparentés sur la base des données des essais cliniques sur le donanemab, des informations de prescription de la FDA et d’autres documents pertinents, ainsi que de l’avis d’experts.
Résultats
Les patients éligibles au traitement par le donanemab doivent présenter les caractéristiques suivantes
- Déficience cognitive légère (MCI) ou démence légère due à la MA : Stades cliniques 3-4 sur l’échelle de détérioration globale et score au Mini-Mental State Examination (MMSE) de 20 à 30 points.
- Preuve de pathologie amyloïde-β confirmée par les biomarqueurs du liquide céphalorachidien (LCR) (rapports amyloïde-β 42/40 ou phosphorylé (p)-tau 181/amyloïde-β 42) ou par la tomographie par émission de positrons (TEP).
- Génotypage de l’apolipoprotéine (apo)E et imagerie par résonance magnétique (IRM) effectués avant le traitement.
Ne sont pas éligibles au traitement par donanemab :
- Patients présentant des signes IRM d’une maladie grave de la substance blanche ou d’une angiopathie amyloïde cérébrale significative, tels que plus de quatre microbleeds, une macrohémorragie de plus d’un centimètre ou une sidérose superficielle.
- Patients prenant des anticoagulants.
Autres recommandations :
- Les thrombolytiques ne doivent pas être utilisés pendant le traitement par le donanemab ; la thrombectomie mécanique est possible.
- Arrêt du donanemab si l’IRM montre une macrohémorragie, plus d’une zone de sidérose superficielle, plus de 10 microhémorragies, plus de deux épisodes d’anomalies d’imagerie liées à l’amyloïde (ARIA) ou des ARIA sévères.
- Envisager l’arrêt du traitement après 12 à 18 mois si la TEP amyloïde de suivi est négative.
M. Rabinovici a précisé qu’il s’agit de “recommandations, pas de lignes directrices ni de critères, et que, comme toujours lorsqu’il s’agit de traiter un patient individuel, c’est le jugement clinique qui prime”.
Admissibilité au traitement anti-amyloïde dans des populations de cliniques de la mémoire en situation réelle (Résumé : OC22)
Présentateur : Anna Matton (Suède)
- Les recommandations d’utilisation appropriées pour le lécanemab ont été appliquées à un échantillon représentatif du monde réel de 2126 patients provenant de sept cliniques de la mémoire en Suède, afin de déterminer qui pourrait bénéficier d’un traitement anti-amyloïde.
Résultats :
- Âge moyen : 77,1 ans ; 50,4 % de femmes.
- Le MMSE moyen était de 27 points.
- 32 % des patients présentaient un score de Fazekas pathologique.
- 62 % d’entre eux souffraient de DCL et 24 % de démence de type Alzheimer.
- 17% des patients prenaient des anticoagulants et 17% des antiplaquettaires.
- Sur les 918 patients pour lesquels des mesures des biomarqueurs du LCR étaient disponibles, 34,3 % présentaient des anomalies de l’amyloïde-β 42, 32,5 % des anomalies de la protéine phosphorylée (p)-tau, 50,4 % des anomalies de la protéine tau totale et 20,6 % des anomalies de la lumière des neurofilaments.
- Les profils ATN de 774 patients étaient les suivants :
| A-T-N- | A–T–N+ | A+T–N+ | A–T+N– | A+T–N– | A–T+N+ | A+T+N– | A+T+N+ |
|---|---|---|---|---|---|---|---|
| 26.1% | 18.5% | 11.8% | 10.7% | 9.6% | 9.3% | 7.0% | 7.1% |
A : CSF Amyloid-β 42 ; T : CSF p-tau181, N : atrophie du lobe temporal médian Les profils surlignés sont ceux qui sont éligibles pour un traitement anti-amyloïde.
- Sur la base des critères d’inclusion et d’exclusion recommandés, 86 personnes étaient éligibles pour un traitement anti-amyloïde, soit 9,4 % des patients éligibles pour la LCR et 4,1 % de l’ensemble des patients.
- Ces patients représentaient 10 % des patients atteints de DCL (64 % au total) et 25 % des patients atteints de démence MA (36 % au total).
“Dans l’ensemble, [une] proportion relativement faible de patients serait potentiellement éligible”, a déclaré M. Matton. “Des approches de dépistage plus larges, incluant les biomarqueurs sanguins de la MA, pourraient potentiellement augmenter le nombre de patients.
Expérience d’un an sur l’utilisation du lécanemab dans la pratique clinique (Résumé : LBS2) Traitement par lécanemab dans des conditions réelles aux États-Unis (Présentation 1)
Présentateur : Marwan Sabbagh
- Données évaluées à partir de la base de données de recherche Komodo pour 3155 patients ayant commencé un traitement par lecanemab (principalement depuis octobre 2023) et ayant une moyenne de 129 jours de suivi et des informations sur l’activité clinique 12 mois avant le traitement.
Résultats
- Les patients avaient un âge moyen de 75 ans, 84,3 % étaient blancs, 93,3 % venaient de zones urbaines, 55,8 % étaient des femmes.
- La majorité d’entre eux présentaient des comorbidités, principalement une dyslipidémie (54,4 %) et une hypertension (45,7 %).
- 60,8 % étaient atteints de DCL et 83,8 % de MA.
- 67,6 % prenaient des médicaments anti-AD par voie orale (inhibiteurs de l’acétylcholinestérase ou mémantine), 3,7 % des anticoagulants et 4,1 % des antiplaquettaires.
- Le délai moyen entre le diagnostic et le début du traitement était de 4,9 mois.
- Les patients ont reçu en moyenne deux perfusions mensuelles à 16,5 jours d’intervalle et la première IRM a été réalisée en moyenne 46,7 jours après le début du traitement.
- Le taux d’adhésion – pas plus de 90 jours entre deux perfusions – était de 85,1 %.
Les patients recevaient le lécanemab “conformément à l’étiquette et dans les délais”, a déclaré Mme Sabbagh. Ils sont “très motivés pour rester sous lecanemab une fois qu’ils ont compris les conséquences du traitement et de l’absence de traitement”.
Utilisation du lécanemab dans la pratique clinique d’un centre médical universitaire (Présentation 2)
Présentateur : Lawrence Honig
- Expérience du traitement de 162 patients par lecanemab au centre médical universitaire Irvine à New York, États-Unis.
Résultats
- Les patients avaient un âge moyen de 73 ans, 90 % étaient blancs et 56 % étaient des femmes.
- Les affections comorbides étaient fréquentes, notamment les accidents vasculaires cérébraux et les hémorragies dans 2 % des cas et les malformations vasculaires dans 3 % des cas.
- Preuve de démence MCI ou AD confirmée par les biomarqueurs du LCR dans 86 % des cas, par la TEP dans 26 % des cas, et par les deux dans 12 % des cas.
- 2 % des patients portaient un stimulateur cardiaque et 1 % prenaient des anticoagulants.
- Le score MMSE moyen était de 23,6 points, allant de 11 à 30 points.
- Le génotypage de l’ApoE a été effectué dans 89 % des cas, tandis que les 11 % restants ont refusé.
- Des discussions sur les risques ont été menées avec tous les patients, et seuls ceux qui présentaient plus de quatre microhémorragies à l’IRM avant le traitement ont été exclus.
- Une moyenne de 13,1 perfusions a été reçue sur une période de 18 mois et jusqu’à quatre examens IRM ont été réalisés après le traitement.
- Neuf examens IRM non programmés ont été effectués en raison d’une suspicion d’ARIA, dont un s’est révélé positif.
- Les taux d’œdème/effusion ARIA (ARIA-E) et de microhémorragie ARIA (ARIA-H) étaient respectivement de 11 % et 5 %.
- L’ARIA-E est généralement apparue tôt, était le plus souvent asymptomatique et s’est résorbée en quelques mois avec la reprise de l’administration du lécanemab.
- Le traitement a été interrompu chez 9 % des patients, principalement en raison d’ARIA-E.
- 16 des 17 cas d’ARIA-E étaient asymptomatiques.
- 8 % des patients ont interrompu le traitement : un avec ARIA-E, deux avec ARIA-H, et un avec ARIA-E et ARIA-H qui est décédé par la suite, ainsi que huit en raison de la charge de travail, du désintérêt, de problèmes d’assurance ou de l’absence de bénéfice, et quatre qui ont été perdus de vue en raison d’un déménagement.
L’expérience clinique avec le lécanemab “n’a pas été très différente de celle des essais cliniques”, a déclaré M. Honig. Il s’est avéré “sûr et gérable” , avec “une large acceptation et une bonne observance de la part des patients”.
ARIA
Principaux enseignements:
- L’adaptation de la dose de donanemab pourrait contribuer à réduire les taux d’ARIA-E.
- La liaison “hors cible” des thérapies anti-amyloïdes à l’angiopathie amyloïde cérébrale plutôt qu’à la plaque amyloïde n’explique peut-être pas les différences dans les taux d’ARIA-E.
- L’IA pourrait contribuer à rendre le codage des événements indésirables plus efficace pour les cliniciens.
- La variabilité de l’IRM ultrarapide n’est pas plus importante que celle des scanners standard.
L’effet de différents schémas posologiques de donanemab sur l’ARIA-E et la diminution de l’amyloïde chez les adultes atteints de la maladie d’Alzheimer symptomatique précoce : résultats primaires de TRAILBLAZER-ALZ 6 (Résumé : OC01)
Présentateur : John Sims (USA)
- L’étude de phase 3b visait à déterminer si la modification du schéma posologique du donanemab pouvait réduire les taux d’ARIA-E chez 843 patients atteints de la maladie d’Alzheimer.
–
–
Titration standard – donanemab intraveineux toutes les 4 semaines à une dose de 700 mg pour les trois premières perfusions, puis à 1400 mg pour la quatrième.
Schéma de titration modifié – donanemab intraveineux 350 mg pour la première perfusion, 700 mg pour la deuxième perfusion, 1050 mg pour la troisième perfusion et 1400 mg pour la quatrième perfusion.
Résultats
- À la semaine 24, les patients du groupe de titrage modifié présentaient un taux d’ARIA-E significativement plus faible que ceux du groupe de titrage standard, soit 13,7 % contre 23,7 %.
- La probabilité d’obtenir une réduction d’au moins 20 % des taux d’ARIA-E avec la titration modifiée était de 94 %, ce qui correspondait à l’objectif principal de l’étude, à savoir plus de 80 %.
- À l’IRM, après 24 semaines, 86 % des patients du groupe de titrage modifié ne présentaient plus d’ARIA-E, contre 76 % des patients du groupe de titrage standard.
- Il n’y a pas eu de différence entre les deux schémas de titration en termes d’autres événements indésirables graves, d’arrêts de traitement ou d’événements indésirables liés au traitement.
- Un décès est survenu chez un patient atteint d’ARIA-E en cours dans le groupe de titration modifiée, en raison d’une hémorragie cérébrale intraparenchymateuse.
- L’abaissement du taux d’amyloïde a été comparable avec les schémas de titration modifié et standard (diminutions moyennes par rapport à la ligne de base de 56,3 et 58,8 centiloïdes, respectivement).
Les résultats suggèrent qu ‘”une approche de titration améliorée peut limiter le risque d’ARIA tout en maintenant une réduction suffisante de l’amyloïde”.
La préférence des anticorps anti-amyloïdes pour les agrégats Aβ vasculaires n’explique pas les taux d’ARIA (Résumé : OC35)
Présentateur : Andrew Stern
- L’affinité avec laquelle l’aducanumab, le donanemab et le lécanemab se lient à l’angiopathie amyloïde cérébrale “hors cible” par rapport à la plaque amyloïde “sur cible” a été testée en tant qu’explication possible des différents taux d’anomalies d’imagerie liées à l’amyloïde avec œdème et/ou épanchement (ARIA-E) parmi les thérapies.
Résultats
- Taux d’ARIA-E rapportés précédemment :
- 35,2 % pour l’aducanumab (*2,8 fois la différence)
- 24,0 % pour le donanemab
- 12,6 % pour le lecanemab (*2,8 fois la différence)

- La liaison préférentielle des anticorps synthétisés à partir de séquences d’acides aminés à l’amyloïde-β 40 méningée, qui est enrichie en CAA, et à l’amyloïde-β42 parenchymateuse, qui est enrichie en plaques, a été augmentée en moyenne :
- 1,51 fois avec l’aducanumab
- 1,63 fois avec le donanemab
- 1,85 fois avec lecanemab
- Il n’y avait pas de différence significative entre les trois traitements, et la liaison préférentielle de 0,83 à 1,8 fois avec l’aducanumab n’explique pas la différence de 2,8 fois dans le taux d’ARIA-E par rapport au lécanemab.
Stern a conclu que “la préférence des anticorps pour les agrégats méningés riches en amyloïde-β 40 par rapport aux agrégats parenchymateux riches en amyloïde-β 42 ne peut pas expliquer les différences dans les taux d’ARIA”.
Surveillance de la sécurité dans les essais cliniques sur la maladie d’Alzheimer grâce à l’intelligence artificielle (Abstract : OC36)
Présentateur : Gustavo Jimenez-Maggiora (USA)
- L’utilisation du traitement du langage naturel et de l’intelligence artificielle (IA) pour améliorer le codage de 980 événements indésirables par les cliniciens a été évaluée à partir de données recueillies dans huit essais cliniques terminés portant sur des patients atteints de la maladie d’Alzheimer symptomatique.
Résultats
- L’IA a surpassé le codage traditionnel basé sur le clinicien dans l’ensemble (précision de 88 contre 71 %) et dans toute la gamme de fréquence des codes, et a amélioré la précision au niveau du rapport (après examen clinique par des experts et analyse biostatistique) de 3 à 13 %.
- Dans une cohorte distincte (étude A4) de patients en phase pré-AD, le codage par l’IA était comparable au codage par le clinicien, à environ 70 %, mais augmentait la précision au niveau de la déclaration de 3 à 5 %.
- Le codage AE basé sur l’IA s’est avéré plus rentable, avec une réduction des coûts d’environ 80 %.
“Le codage basé sur l’intelligence artificielle peut être effectué instantanément sans perte de précision par rapport au codage par le clinicien, ce qui permet de réduire les coûts et d’améliorer la disponibilité des données de sécurité”, a déclaré M. Jimenez-Maggiora.
Un protocole d’IRM ultra-rapide pour faciliter le diagnostic et le traitement de la maladie d’Alzheimer (Abstract : OC34)
Présentateur : Miguel Rosa-Grilo (Royaume-Uni)
- La variabilité de l’interprétation par trois neurologues d’un examen d’imagerie rapide utilisant l’imagerie parallèle avancée à ondes contrôlées a été comparée à celle d’un examen clinique standard d’imagerie par résonance magnétique (IRM) (examens rapides vs examens standards) chez 90 personnes : 41,1 % n’avaient pas de maladie cérébrale neurodégénérative ; 21,1 % avaient la MA ; 12,2 % avaient une dégénérescence lobaire frontotemporale (DLFT) ; 8,9 % avaient une déficience cognitive vasculaire (DCV) ; et 16,7 % avaient d’autres diagnostics.
Résultats
- Le balayage rapide réduit le temps d’acquisition d’environ 63 % par rapport à un balayage standard (6 min 29 s contre 17 min 39 s).
- La variabilité introduite par la scintigraphie rapide était inférieure à celle de la scintigraphie standard, ce qui prouve la non-infériorité des deux méthodes.
Les coefficients kappa de fiabilité inter-évaluateurs* étaient les suivants :
- Normal : Balayage rapide=0,61 ; balayage standard=0,65 ; entre les balayages : 0,80
- AD : balayage rapide=0,38 ; balayage standard=0,42 ; entre les balayages=0,72
- FTLD : balayage rapide = 0,79 ; balayage standard = 0,71 ; entre les balayages = 0,95
- ICV : balayage rapide=0,75 ; balayage standard=0,75 ; entre les balayages=0,95
- Autres diagnostics : Scintigraphie rapide=0,48 ; scintigraphie standard=0,50 ; entre les scintigraphies=0,76
* 0,21-0,40=faible ; 0,41-0,60=modéré ; 0,61-0,80=substantiel
“D‘autres études sont nécessaires pour évaluer les gains de temps réels dans la pratique et les mises en œuvre ultra-rapides dans différents champs d’application”, a déclaré M. Rosa-Grilo.
Cliquez ci-dessous pour télécharger le Microdigest 3 pdf du CTAD :
Download Microdigest 3 FR PDFVous pouvez également télécharger le Microdigest 2 pdf du CAAA :
Download Microdigest 2 FR PDFVous pouvez également télécharger le Microdigest d’AD/PD & CONy :
Download Microdigest 1 FR PDF





