微摘 3
CTAD 综述
在此,我们总结了 2024 年 CTAD 发布的主要数据,重点关注新型生物标记物和抗淀粉样蛋白疗法。
临床试验筛选
主要启示
- p-tau217 比值是降低所有种族和民族群体中淀粉样蛋白-β 正电子发射断层扫描(PET)筛查失败率的合适生物标志物。
- 较低的血浆合格率表明,淀粉样蛋白异常在代表性不足的种族和民族群体中的流行率不同,这也是导致他们在抗淀粉样蛋白治疗试验中代表性不足的原因。
- Tau PET 是与认知密切相关的良好试验终点。
AHEAD 3-45 研究:临床前抗抑郁试验的新型筛选过程的设计与结果(摘要:LBS1)
AHEAD 3-45 研究包括两项姊妹试验:
- A3 是一项为期 4 年的 2 期试验,针对淀粉样蛋白-β PET 中等水平(20-40 centiloids[CL] )、认知功能未受损的患者,进行静脉注射莱卡尼单抗(5 毫克/千克滴定,然后每月 10 毫克/千克,共 208 周)与安慰剂的对比试验。目的是在 4 年时间内防止认知能力下降(临床前阿尔茨海默氏症认知能力综合指数 5[PACC-5] )。
- A45 是一项为期 4 年的 3 期试验,针对淀粉样蛋白-β PET 阳性(≥40 CL)、认知功能未受损的患者,采用静脉注射来卡尼单抗(5 毫克/千克,双周一次,共 6 周,然后 10 毫克/千克,双周一次,共 86 周,然后每月一次,共 120 周)与安慰剂的对比试验。目的是减缓淀粉样蛋白-β的积累(淀粉样蛋白PET和tau PET)。
筛选期刚刚结束。
AHEAD 3-45 研究中的血浆生物标志物筛查、淀粉样蛋白和 tau PET 成像(演讲 2)
演讲者:Reisa Sperling(美国)
- A3 和 A45 的筛选过程:
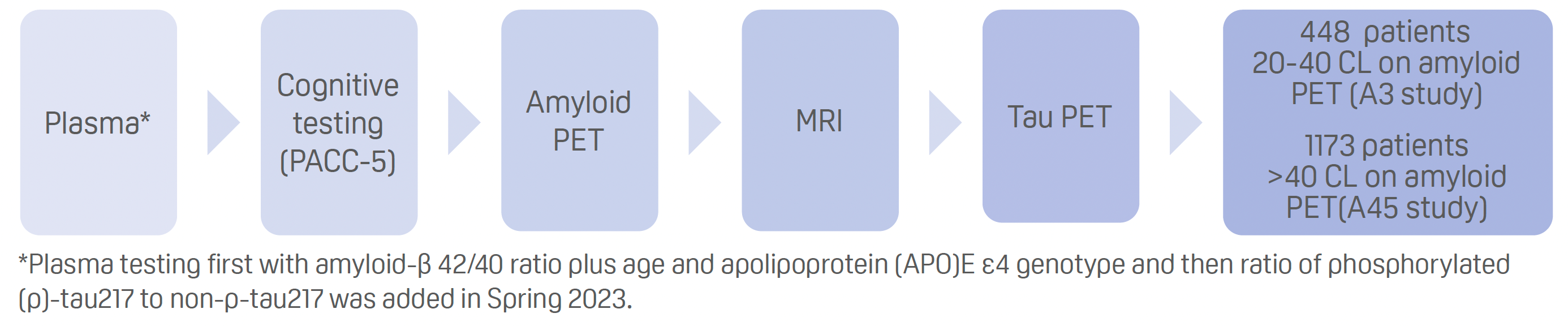
结果
- 通过血浆检测淀粉样蛋白-β42/40比值,可将预测超过11个CL的淀粉样蛋白PET失败率从约75%降至约55%。
- 加入 p-tau217 比值后,预测 18 CL 以上的淀粉样蛋白 PET 失败率进一步降至约 40-45%。
- 血浆 p-tau217 比值与 20 CL 资格的淀粉样蛋白 PET 的接收器操作特征曲线下面积之比达到 0.95。
- 使用全血浆检测模型进行血浆检测,可将预测 40 CL 以上的淀粉样蛋白 PET 失败率降至 25%。
- A45 研究人员的颞叶内侧和新皮质 tau PET 均高于 A3 研究人员。
- 在 PACC-5 中,Tau PET 与认知的相关性最强。
“p-tau217比值的早期升高可能有助于更早开展旨在预防未来淀粉样蛋白阳性的干预试验,” Sperling说。 “研究结果支持将tau PET作为关键终点,作为A3和A45成像、生物标志物和认知之间的潜在桥接结果”。
临床前注意力缺失症试验中血浆 p-tau217 生物标志物合格率的种族和民族差异(演讲 3)
演讲者多丽丝-莫利纳-亨利
- 了解血浆生物标志物算法在加入 p-tau 217 比值的窗口期检测不同种族和族裔中 18 CL 以上淀粉样蛋白 PET 合格性的能力。
结果
- 与非西班牙裔白人成年人相比,所有代表性不足的种族和民族群体的血浆合格率都较低。
- 不同种族/族裔群体的 PET 合格率相当,没有显著差异。
| 种族/族裔群体 | 人数 | 血浆合格率 | 符合血浆资格且同时符合 PET 资格的患者百分比 |
|---|---|---|---|
| 非西班牙裔白人 | 4832 | 27% | 71% |
| 西班牙裔 白人 | 877 | 19% | 63% |
| 西班牙裔 黑人 | 62 | 11% | 75% |
| 非西班牙裔 亚洲人 | 155 | 15% | 50% |
| 非西班牙裔黑人 | 511 | 19% | 68% |
“Henry说:“较低的血浆合格率表明,淀粉样蛋白异常在这些群体中的发生率不同[……],这表明在种族和民族上代表性不足的群体中,淀粉样蛋白水平较低,导致他们在抗淀粉样蛋白试验中代表性不足 。
“她补充说:“各组 PET 的合格率相同,证明相同的血浆预测算法在不同种族和族裔群体中得到了适当应用 。
“这表明[……]其他因素可能是淀粉样蛋白发病率较低的种族和民族群体中痴呆症风险较高的原因”。
生物标记物和注意力缺失症诊断
主要启示
- β-突触核蛋白可能是阿尔茨海默病(AD)中一种新的基于突触血液的生物标记物。
- 临床痴呆评定量表-方格总和每 0.5 个单位所花费的时间有助于评估治疗反应。
- 多分析血液生物标志物检测可能有助于诊断决策。
- 需要解决淀粉样蛋白正电子发射断层扫描(PET)阳性率和诊断时临床阶段的种族/族裔差异问题,以改善治疗的可及性。
- 需要制定策略,以便在慢性肾病等合并症的情况下解释 p-tau217 的表现。
- 以血液为基础的生物标志物的不同作用可为循序渐进的AD诊断方法铺平道路。
- 如果脑脊液(CSF)和 PET 测量的淀粉样蛋白-β阳性率不同,建议在推荐抗淀粉样蛋白治疗前进行进一步检测。
无症状的常染色体显性阿尔茨海默病患者突触血液标记物 β-突触核蛋白的早期增加(摘要 ID OC14 阿尔茨海默病(摘要 ID OC14)
演讲者Patrick Oeckl(德国)
- 免疫沉淀质谱法用于定量检测178名参加显性遗传性阿尔茨海默氏症网络(DIAN)研究者血液样本中的突触前蛋白β-突触核蛋白。
- 其中包括 31 名有症状的基因突变携带者、78 名无症状的基因突变携带者和 69 名认知功能未受损的基因突变非携带者。
结果
- 在无症状的常染色体显性遗传性痴呆症患者中,β-突触核蛋白水平明显高于认知功能未受损的个体,而在有症状的患者中,β-突触核蛋白水平最高。
- 突变携带者血液中的β-突触核蛋白水平在症状出现前约11年开始上升。
- 根据变异携带者和非携带者的体液生物标志物水平出现明显差异的时间从早到晚进行排序:
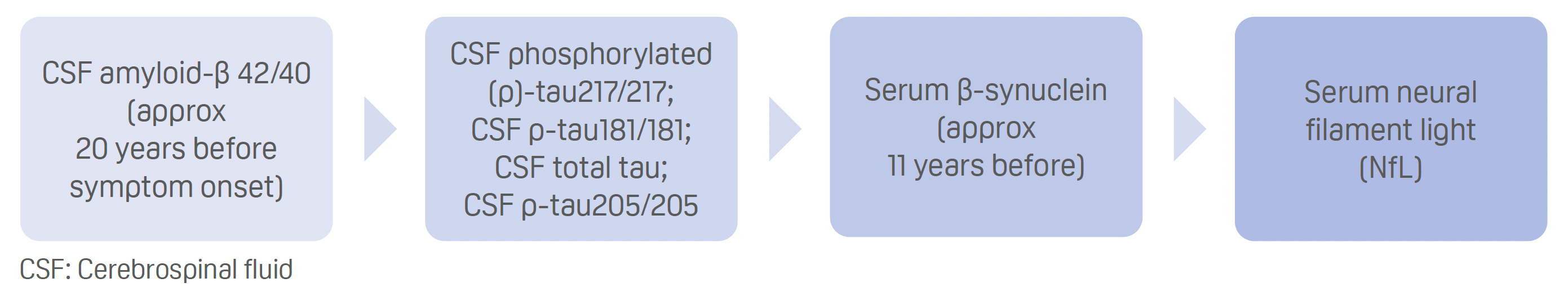
- 血清β-突触核蛋白轨迹先于认知障碍、脑萎缩和代谢低下的成像测量。
- 血清β-突触核蛋白预测淀粉样β阳性的能力适中(接收器操作特征曲线下面积为 0.75)。
- 血清β-突触核蛋白与认知障碍有明显相关性。
Oeckl说:“血液β突触核蛋白可以成为一种 “易于获取的突触标记物,用于诊断、预后、[and] 药物开发” 。
CDR-SB的临床进展:DIAN和ADNI队列中每个级别的停留时间(摘要OC19)
演讲者王国桥(美国)
- 在两个队列–DIAN(常染色体显性缺失性痴呆)和ADNI(散发性缺失性痴呆)–中,使用疾病进展随机效应模型研究了患者在每0.5个单位的临床痴呆分级量表–方框总和(CDR- SB)上停留的时间长度(称为停留时间)。
结果
- 常染色体显性 AD:当 CDR-SB 达到 3 点或更高时,每 0.5 个 CDR-SB 单位的停留时间为 0.5 年或更短。
- 零星 AD:当 CDR-SB 达到 3.5 分或以上时,每 0.5 个 CDR-SB 单位的居住时间为 0.5 年或更短。
- 从 CDR-SB 评分 0.5 分到 3.5 分的停留时间:常染色体显性 AD 平均为 6.5 年,散发性 AD 平均为 5.6 年,两者相差约 0.9 年。
例如,利用滞留时间,可以计算出莱卡尼单抗(lecanemab)Clarity AD 试验开放标签扩展阶段患者的治疗效果:
- 基线 CDR-SB 评分为 3.17 分,据估计,安慰剂治疗的患者需要 2.3 年才能下降 3.09 分,而莱卡尼单抗治疗的患者则需要 3.0 年,即疾病进展延迟 0.7 年。
CDR-SB 中每个 0.5 单位水平的停留时间 “可以为解释和评估治疗效果提供一种标准化的替代方法,”Wang 说。
脑淀粉样蛋白升高的 CSF 和 PET 测定之间的差异及其预后意义(摘要:LB10)
演讲者戴维-克诺普曼(美国)
- 我们对 ADNI 队列中的 587 名轻度认知障碍患者进行了认知功能下降评估,这些患者的淀粉样蛋白-β 阳性的 CSF 和 PET 测量结果不一致。
结果
- 测试结果不一致的情况并不常见,发生率约为 5%。
- CSF和PET淀粉样蛋白检测结果均为阴性的患者和检测结果不一致的患者(任一检测结果均为阴性)在基线时的认知能力相似,与两种检测结果均为阳性的患者相比,认知能力更强。
- 对于CSF淀粉样蛋白检测呈阳性而PET淀粉样蛋白检测不呈阳性的患者,CSF p-tau/淀粉样蛋白-β比率大大低于两种检测指标均呈阳性的患者。
- 在中位 4 年的随访中,测试结果不一致的患者在雷伊听觉言语学习测试 1-6 试验总和或临床痴呆评定量表-方框总和上的得分并没有显著下降,这与在这两项测试中均呈阳性的患者不同。
- 在随访过程中,只有在两项检测结果均呈阳性的患者中,痴呆症的发病率才会明显升高(每 100 人年 17.3 例),而两项检测结果均呈阴性或不一致的患者的发病率相近(每 100 人年 1.9 例至 3.0 例不等)。
“Knopman说:“由于CSF阳性/PET阴性的MCI患者并没有表现出群体性的衰退,因此在推荐他们接受抗淀粉样蛋白单克隆抗体治疗之前,应该获得更多关于疾病进展可能性的证据。
评估多分析血液生物标志物检测对认知障碍的影响:QUIP II 临床实用性研究的结果(摘要 OC32)
演讲者乔尔-布劳恩斯坦(美国)
- 对治疗 203 名认知障碍患者的 12 名临床医生进行了调查,以评估 PrecivityAD2(C2N Diagnostics,美国密苏里州圣路易斯市)在临床管理和决策中的使用情况。
- 血液检测可量化血浆中淀粉样蛋白-β42 和 40 以及 p-tau217 和非 tau217 的水平,从而得出淀粉样蛋白概率评分(APS)2,评分范围为 0-100 分,其中 0-47 分表示结果为阴性,淀粉样蛋白阳性的可能性较低;48-100 分表示结果为阳性,淀粉样蛋白阳性的可能性较高。
结果
- 51%的患者检测结果呈阴性。
- 99% 符合预期用途。
- AD 诊断确定性、药物治疗或进一步脑淀粉样蛋白评估的 75% 变化。
- 在使用血液检测前,APS2 结果与临床医生报告的注意力缺失症概率之间的相关性较弱,而在使用血液检测后,两者之间的相关性较强。
- 对于阴性患者,临床医生报告的 AD 概率从使用血液检测前的 53% 降至 11%,而对于阳性患者,则从 65% 升至 93%。
- 使用血液检测前后,阴性患者的 AD 药物处方明显减少,而阳性患者的 AD 药物处方则明显增加。
- 额外的脑淀粉样蛋白检测结果阴性患者减少了 70%,阳性患者减少了 26%。
“我们相信[……]PrecivityAD2™ 血液检测会对认知障碍患者的诊断确定性、药物治疗管理和额外的淀粉样蛋白评估决策带来有临床意义的改变,” Braunstein 说。
演讲者吉尔-拉宾诺维奇(美国)
不同种族/族裔在淀粉样蛋白 PET 检测结果和健康的社会决定因素方面的差异:New IDEAS 的研究结果(摘要 OC08)
- 我们对 4845 名患有轻度认知障碍 (MCI; 64%) 或痴呆症 (37%) 的新 IDEAS 参与者的淀粉样蛋白 PET 阳性率、临床阶段和健康的社会决定因素进行了比较,其中 21% 的参与者自我认同为黑人/非裔美国人 (BAA),18% 为拉丁裔/西班牙裔 (LAT),61% 为其他种族或族裔 (NBL)。
成果
BAA 和 LA 小组分别是
- 淀粉样蛋白-PET阳性率分别为60.7%、60.8%和68.2%,比NBL组低28%;
- 更有可能患有血管并发症,如高血压(73.3% 和 61.5% 对 54.3%)和糖尿病(29.9% 和 29.8% 对 16.3%);
- 相对于 MCI,NBL 组更有可能出现痴呆,比例分别为 47.4% 和 43.5% 对 30.5%;
- 更有可能出现非典型表现,因此更难诊断(36.0% 和 35.55 vs 26.6%);
- 与 NBL 组相比,基线平均迷你精神状态检查得分更低(21 分和 21 分比 25 分)。
“拉比诺维奇说:“解决这些可改变的差异对于提高医疗服务的公平性和痴呆症预防战略的实施至关重要 。
非裔美国人队列中血浆 p-tau217 的表现:非裔美国人中年抗击阿尔茨海默氏症研究的发现(摘要:OC13)
演讲者吉尔达-恩尼斯(美国)
- 我们评估了血浆 p-tau217 检测淀粉样蛋白 PET 阳性的准确性,研究对象是 AA-FAIM 队列中 233 名认知功能未受损的成年人,他们被认定为非西班牙裔黑人或非裔美国人,且至少患有以下一种并发症:肾功能受损、心血管疾病、高血压、糖尿病或肥胖症。
成果
- 较高的血浆 p-tau217 水平与轻度(估计肾小球滤过率[eGFR] 低于 90 mL/min 每 1.73m2)和中重度(eGFR 低于 60 mL/min 每 1.73m2)肾功能损害以及心血管疾病(心肌梗死、中风或充血性心力衰竭)明显相关。
- 在分别为 38 人和 64 人的小样本中,这两种关联都无法用淀粉样蛋白负荷来解释。
- 在对年龄和性别进行控制后,血浆中p-tau217的水平在患有1期或2期高血压、糖尿病或肥胖症的患者中没有明显升高。
- 在AA-FAIM队列的65名患者中,以0.35 pg/mL为临界点,血浆p-tau217检测淀粉样蛋白PET阳性的准确率为90%,灵敏度为94%,特异性为80%(全球AD首席执行官倡议建议在初级医疗中使用血液生物标记物的准确率分别为90%和85%)。
“Ennis说:“我们需要研究一些策略,以便在p-tau217假性增高或假性降低的医疗条件下准确解读血浆p-tau217 。
阿尔茨海默病血浆生物标志物在逐步生物标志物引导诊断中的不同作用:亚洲人群的正面比较(摘要:OC38)
演讲者Daeun Shin(大韩民国)
- 我们对 2984 名亚洲人(22% 认知功能未受损,68% AD 认知功能受损,6% 皮层下血管认知功能受损,3% 额颞叶痴呆)的血浆标志物的不同作用进行了研究,以了解它们是否可用作更有效的生物标志物引导的 AD 诊断步骤策略的一部分。
- 研究的血浆生物标志物:淀粉样蛋白-β 42/40;p-tau181;p-tau217;p-tau231;GFAP;NfL。
成果
| 最佳生物标志物 | 作用 | AUC |
|---|---|---|
| NfL | 将任何认知障碍患者与无认知障碍患者区分开来 | 0.71–0.94 |
| p-tau217 | 区分所有组别中的淀粉样蛋白-β PET 阳性率 | 0.88–0.95 |
| p-tau217 | 在认知功能受损的 AD 患者中区分 tau PET 阳性 | 0.90–0.91 |
| p-tau217 | 将淀粉样蛋白-β PET阳性的AD认知障碍患者与淀粉样蛋白-β PET阴性的非AD痴呆患者区分开来。 | 0.94–0.95 |
| p-tau217和GFAP | 预测认知功能未受损患者的认知功能下降 | 不适用 |
AUC:接收者操作特征曲线下的面积;N/A:不适用;NfL:神经丝光;p:磷酸化;PET:正电子发射断层扫描;GFAP:神经胶质纤维酸性蛋白
“这些发现强调了阿尔茨海默病血浆生物标志物在逐步诊断方法中的不同作用的重要性,”Shin 说。 Shin说。
抗淀粉样蛋白疗法
主要启示
- 已针对多那尼单抗发布了适当使用建议,以帮助确定合适的治疗对象。
- 接受抗淀粉样蛋白治疗的资格相对较低,通过更广泛的筛查(包括基于血液的生物标志物)有可能得到改善。
- 现实世界中的患者正在按照 FDA 批准的标签信息进行适当选择和接受莱卡奈单抗。
- 在临床上,患者对莱卡尼单抗的耐受性很好,依从率也很高。
多奈单抗:适当使用建议(摘要:LB01)
演讲者吉尔-拉宾诺维奇(美国)
- 这些建议是由注意力缺失症及相关疾病治疗工作组根据多那尼单抗临床试验数据、FDA 处方信息和其他相关文献以及专家意见制定的。
成果
符合 Donanemab 治疗条件的患者应具备以下条件
- 轻度认知障碍(MCI)或因注意力缺失导致的轻度痴呆:整体恶化量表(Global Deterioration Scale)临床 3-4 期,迷你精神状态检查(Mini-Mental State Examination,MMSE)得分 20-30 分。
- 通过脑脊液(CSF)生物标记物(淀粉样β 42/40 或磷酸化(p)-tau 181/ 淀粉样β 42 比率)或正电子发射断层扫描(PET)确认淀粉样β病理学证据。
- 治疗前进行载脂蛋白 (apo)E 基因分型和磁共振成像 (MRI)。
不符合多那尼单抗治疗条件的人员包括
- 核磁共振成像显示有严重白质病变或明显脑淀粉样血管病的患者,如超过 4 个微小出血点、超过 1 厘米的大出血或浅表巩膜病变。
- 服用抗凝剂的患者。
进一步建议
- 在多那尼单抗治疗期间,不应使用血栓溶解剂;机械血栓切除术是可行的。
- 如果磁共振成像显示任何大出血、一个以上表层巩膜病变区域、10 个以上微出血、两次以上淀粉样蛋白相关成像异常 (ARIA) 或严重 ARIA,则停用多奈单抗。
- 如果淀粉样蛋白 PET 随访呈阴性,考虑在 12-18 个月时停止治疗。
拉比诺维奇说,这些都是 “建议,它们不是指南或标准,在治疗个体病人时,临床判断始终是最重要的”。
现实世界中记忆门诊人群接受抗淀粉样蛋白治疗的资格(摘要:OC22)
演讲者安娜-马顿(瑞典)
- 莱卡奈单抗的适当使用建议适用于来自瑞典七家记忆诊所的 2126 名具有代表性的真实患者样本,以确定哪些患者符合抗淀粉样蛋白治疗的条件。
结果
- 平均年龄 77.1 岁;50.4% 为女性。
- MMSE 平均值为 27 分。
- 32% 的患者有病理性 Fazekas 评分。
- 62% 患有 MCI,24% 患有 AD 痴呆症。
- 17% 的患者服用抗凝剂,17% 的患者服用抗血小板药物。
- 在918名可测量脑脊液生物标志物的患者中,34.3%的患者淀粉样蛋白-β 42异常,32.5%的患者磷酸化(p)-tau异常,50.4%的患者总tau异常,20.6%的患者神经丝光异常。
- 其中 774 名患者的 ATN 资料如下:
| A-T-N- | A–T–N+ | A+T–N+ | A–T+N– | A+T–N– | A–T+N+ | A+T+N– | A+T+N+ |
|---|---|---|---|---|---|---|---|
| 26.1% | 18.5% | 11.8% | 10.7% | 9.6% | 9.3% | 7.0% | 7.1% |
A:CSF 淀粉样蛋白-β 42;T:CSF p-tau181;N:颞叶内侧萎缩 高亮显示的是符合抗淀粉样蛋白治疗条件的病例。
- 根据推荐的纳入和排除标准,有86人符合抗淀粉样蛋白治疗条件–占CSF合格患者的9.4%,占患者总数的4.1%。
- 这些患者占 MCI 患者的 10%(共 64%),占 AD 痴呆症患者的 25%(共 36%)。
“Matton说:“总体而言,符合条件的患者比例相对较低 。“包括AD血液生物标志物在内的更广泛的筛查方法有可能会增加患病人数”。
在临床实践中使用来卡尼单抗的一年经验(摘要:LBS2 美国现实环境中的来卡尼单抗治疗(演讲 1)
演讲者马万-萨巴格
- 从 Komodo 研究数据库中评估了 3155 名患者的数据,这些患者已开始莱卡奈单抗治疗(主要自 2023 年 10 月起),平均随访 129 天,并提供了治疗前 12 个月的临床活动信息。
成果
- 患者平均年龄为 75 岁,84.3% 为白人,93.3% 来自城市地区,55.8% 为女性。
- 大多数人有合并症,主要是血脂异常(54.4%)和高血压(45.7%)。
- 60.8%的人患有 MCI,83.8%的人患有 AD。
- 67.6%的人正在口服抗逆转录酶药物(乙酰胆碱酯酶抑制剂或美金刚),3.7%的人正在服用抗凝剂,4.1%的人正在服用抗血小板药物。
- 从诊断到开始治疗的平均时间为 4.9 个月。
- 患者平均每月在 16.5 天内进行两次输液,首次磁共振成像扫描平均在治疗开始后 46.7 天进行。
- 两次输液间隔不超过 90 天的坚持率为 85.1%。
Sabbagh说,患者“按时按标签 “接受利卡单抗治疗。他们“一旦了解了治疗和不治疗的后果,就会非常积极地坚持使用利卡尼单抗”。
一家学术医疗中心在临床实践中使用来卡尼单抗(演讲 2)
演讲者劳伦斯-霍尼格
- 美国纽约欧文学术医学中心用莱卡尼单抗治疗 162 名患者的经验。
成果
- 患者的平均年龄为 73 岁,90% 为白人,56% 为女性。
- 合并症很常见,其中中风和出血占 2%,血管畸形占 3%。
- 通过 CSF 生物标记物确诊 MCI 或 AD 痴呆症的占 86%,通过 PET 确诊的占 26%,同时通过这两项确诊的占 12%。
- 2%的患者安装了心脏起搏器,1%的患者正在服用抗凝血剂。
- MMSE 平均分为 23.6 分,从 11 分到 30 分不等。
- 89%的人进行了载脂蛋白E基因分型,其余11%的人则拒绝接受。
- 与所有患者进行了风险讨论,只有那些在治疗前的磁共振成像中出现四次以上微出血的患者被排除在外。
- 在 18 个月的时间里,平均接受了 13.1 次输液,并进行了多达四次治疗后核磁共振扫描。
- 由于怀疑有 ARIA,进行了九次计划外核磁共振扫描,其中一次呈阳性。
- ARIA水肿/渗出(ARIA-E)和ARIA微出血(ARIA-H)的发生率分别为11%和5%。
- ARIA-E通常发生较早,大多无症状,在恢复莱卡奈单抗用药几个月后即可缓解。
- 有 9% 的患者暂停了治疗,主要原因是 ARIA-E。
- 17 例 ARIA-E 中有 16 例没有症状。
- 8%的患者中断了治疗:1 名患者接受了 ARIA-E,2 名患者接受了 ARIA-H,1 名同时接受 ARIA-E 和 ARIA-H 治疗的患者随后死亡,8 名患者因负担过重、不感兴趣、保险问题或缺乏益处而中断治疗,4 名患者因搬迁而失去随访机会。
霍尼格说,莱卡奈单抗的临床经验 “与临床试验中的情况并无二致” 。它 “安全、可控” ,“患者广泛接受并遵从 ” 。
ARIA
主要启示
- 多奈单抗的剂量滴定有助于降低 ARIA-E 的发生率。
- 抗淀粉样蛋白疗法与脑淀粉样蛋白血管病变而非淀粉样蛋白斑块的 “脱靶 “结合可能无法解释ARIA-E发生率的差异。
- 人工智能可帮助临床医生提高不良事件编码的效率。
- 超快磁共振成像的变异性并不比标准扫描大。
不同多奈单抗给药方案对早期症状性阿尔茨海默病成人患者降低ARIA-E和淀粉样蛋白含量的影响:TRAILBLAZER-ALZ 6的主要结果(摘要:OC01)
演讲者约翰-西姆斯(美国)
- 这项 3b 期研究考察了修改多那尼单抗的给药方案是否能降低 843 名注意力缺失症患者的 ARIA-E 发生率。
–
–
标准滴注–每 4 周一次静脉注射多奈单抗,前三次输注剂量为 700 毫克,第四次输注剂量为 1400 毫克。
修改滴注方案–静脉注射多那尼单抗,第一次输注 350 毫克,第二次输注 700 毫克,第三次输注 1050 毫克,第四次输注 1400 毫克。
成果
- 到第 24 周时,改良滴定治疗组患者的 ARIA-E 发生率明显低于标准滴定治疗组,分别为 13.7% 和 23.7%。
- 采用修改后的滴定法,ARIA-E 发生率至少降低 20% 的概率为 94%,达到了 80% 以上的主要研究目标。
- 在 24 周的核磁共振成像中,修改滴定组中 86% 的患者没有出现 ARIA-E,而标准滴定组中的这一比例为 76%。
- 在其他严重不良事件、治疗中止或治疗相关不良事件方面,两种滴定方案没有差异。
- 在改良滴定组中,一名正在接受ARIA-E治疗的患者因脑实质内出血而死亡。
- 改良滴定方案和标准滴定方案降低淀粉样蛋白的效果相当(与基线相比,平均降幅分别为 56.3 厘泊和 58.8 厘泊)。
结果表明,“加强滴定方法可限制 ARIA 风险,同时保持足够的淀粉样蛋白减少量”。
抗淀粉样蛋白抗体对血管Aβ聚集体的偏好并不能解释ARIA的发生率(摘要:OC35)
演讲者安德鲁-斯特恩
- 我们测试了阿杜单抗、多那尼单抗和来卡尼单抗与 “脱靶 “脑淀粉样血管病的亲和力,而不是与 “靶上 “斑块淀粉样蛋白的亲和力,以此来解释这些疗法之间不同的淀粉样蛋白相关成像异常水肿和/或渗出(ARIA-E)率。
成果
- 以前报告的 ARIA-E 比率:
- 阿杜单抗为 35.2%(*2.8 倍的差异)
- 多奈单抗为 24.0
- 莱卡奈单抗为 12.6%(*2.8 倍的差异)

- 根据氨基酸序列合成的抗体与脑膜淀粉样蛋白-β 40(富含 CAA)和实质淀粉样蛋白-β42(富含斑块)的优先结合率平均增加:
- 阿杜单抗为1.51倍
- 多那尼单抗的 1.63 倍
- 莱卡奈单抗为1.85倍
- 三种疗法之间没有明显差异,阿杜单抗的优先结合率为 0.83 至 1.8 倍,这并不能解释与莱卡奈单抗相比 ARIA-E 的结合率相差 2.8 倍的原因。
斯特恩得出结论说:“抗体对脑膜淀粉样蛋白-β 40 富集物的偏好超过了对实质淀粉样蛋白-β 42 富集物的偏好,这不能解释 ARIA 发生率的差异”。
阿尔茨海默病临床试验中的人工智能安全监测(摘要:OC36)
演讲者古斯塔沃-希门尼斯-马乔拉(美国)
- 我们评估了使用自然语言处理和人工智能(AI)来增强临床医生对 980 例不良事件的编码能力的情况,这些不良事件是利用从八项针对有症状的注意力缺失症患者的已完成试验中收集的数据进行编码的。
成果
- 人工智能在整体上(准确率 88% 对 71%)和整个编码频率范围内的表现都优于传统的基于临床医生的编码,在报告层面(经过专家临床审查和生物统计分析后)的准确率提高了 3-13%。
- 在另一个队列(A4 研究)中,AI 编码与临床医生编码的准确率相当,约为 70%,但在报告水平上,准确率提高了 3-5%。
- 基于人工智能的 AE 编码更具成本效益,可降低约 80% 的成本。
“Jimenez-Maggiora 说:“基于人工智能的编码可以即时执行,不会损失临床医生编码的准确性,从而降低成本,提高安全数据的可用性 。
帮助诊断和治疗阿尔茨海默病的超快速磁共振成像方案(摘要:OC34)
演讲者米格尔-罗萨-格里罗(英国)
- 在 90 名患者中,比较了三名神经科医生对使用波控高级平行成像技术的快速成像扫描与标准临床磁共振成像(MRI)扫描(快速扫描与标准扫描)的判读差异:41.1%的人没有神经退行性脑病;21.1%的人患有注意力缺失症;12.2%的人患有额颞叶变性(FTLD);8.9%的人患有血管性认知障碍(VCI);16.7%的人有其他诊断。
成果
- 与标准扫描相比,快速扫描可将采集时间缩短约 63%(6 分 29 秒对 17 分 39 秒)。
- 与标准扫描相比,快速扫描带来的变异性更小,这为两种方法的非劣效性提供了证据。
评分者之间的可靠性卡帕系数*为
- 正常:快速扫描=0.61;标准扫描=0.65;两次扫描之间:0.80
- AD:快速扫描=0.38;标准扫描=0.42;两次扫描之间=0.72
- FTLD:快速扫描=0.79;标准扫描=0.71;两次扫描之间=0.95
- VCI:快速扫描=0.75;标准扫描=0.75;两次扫描之间=0.95
- 其他诊断快速扫描=0.48;标准扫描=0.50;两次扫描之间=0.76
* 0.21-0.40=一般;0.41-0.60=中等;0.61-0.80=严重
“Rosa-Grilo 说:“还需要进一步研究,以评估在实践中实际节省的时间,以及在不同场强下的超快实施情况 。
点击以下链接,从 CTAD 下载 Microdigest 3 pdf:
下载 Microdigest 3 中文版 PDF您还可以从 AAIC 下载 pdf 版本的 Microdigest 2:
下载 Microdigest 2 中文版 PDF您还可以从 AD/PD & CONy 下载 Microdigest:
下载 Microdigest 1 中文版 PDF





