微摘 2
AAIC 综述
在此,我们总结了 AAIC 2024 发布的主要数据,重点是新型生物标记物和抗淀粉样蛋白疗法。
血浆 生物标志物
主要启示
潜在的临床应用:
- 临床筛查和选择接受治疗的病人。
- 疾病分期。
- 监测治疗反应。
考虑因素:
- 慢性肾病等合并症的潜在影响。
- 种族差异对检测水平和临界点的影响。
- 需要将临床相关的检测标准化。
- 何时测试
评估阿尔茨海默病血液生物标志物在初级和中级医疗中的前瞻性应用(摘要编号:88404)
演讲者Oskar Hansson(瑞典)
检测血浆生物标志物:
- 淀粉样蛋白概率评分(APS)2:血浆淀粉样蛋白-β 42 与 40 的比率+血浆磷酸化(p)-tau217 与非-tau217 的比率。
- 仅血浆 p-tau217 与非 tau217 的比率。
Results:
- 仅血浆 p-tau217 比值的准确性与 APS2 相当。
- 这两种血浆生物标志物在初级和二级医疗机构、单批次和前瞻性分析、使用单阈值和双阈值临界值、脑脊液(CSF)淀粉样病理学和临床 AD 的诊断准确率约为 89% 至 92%。
- 阳性和阴性预测值(PPV 和 NPVS)分别为 86% 至 92% 和 90% 至 97%。
- 血液生物标志物明显改善了初级保健医生和痴呆症专家的标准诊断工作。
- 根据 95%特异性(高风险)和 95%敏感性(低风险)的双重阈值,”中间 “患者的比例较低:初级医疗机构为 4-13%,二级医疗机构为 6-11%。
血浆生物标志物在 1Florida 阿尔茨海默病研究中心(ADRC)脑淀粉样蛋白筛查中的实用性(摘要编号:91578)
演讲者兰詹-杜阿拉(美国)
- 参与者的民族/种族:56% 西班牙裔和 96% 白人;3% 黑人;1% 其他。
- 测试的血液生物标记物包括:淀粉样蛋白-β 42/40 比率、p-tau217、神经纤维酸性蛋白(GFAP)和神经丝光(NfL)。
- 在逻辑回归模型中,使用尤登指数敏感性和特异性临界值并考虑年龄和性别因素,生物标志物、APOE基因型和海马萎缩的组合预测淀粉样蛋白正电子发射断层扫描(PET)阳性的准确性很高。
- 作为一种独立的血浆生物标记物,p-tau217 的表现最佳。
| AUC | Sensitivity | Specificity | |
|---|---|---|---|
| APOE ε4+, hippocampal atrophy+ (base) | 0.78 | 71% | 76% |
| Base plus all plasma biomarkers | 0.96 | 93% | 87% |
| Base plus amyloid-β 42/40 ratio | 0.88 | 80% | 82% |
| Base plus p-tau217 | 0.94 | 92% | 84% |
| p-tau217 | 0.92 | 85% | 89% |
| Amyloid-β 42/40 ratio | 0.82 | 77% | 81% |
| Amyloid-β 42/40 ratio plus p-tau217 | 0.94 | 93% | 85% |
缩写:AUC:接收者操作特征曲线下的面积;APOE:载脂蛋白 E。
使用血浆 p-tau217 作为预筛方法检测认知功能未受损参与者的淀粉样蛋白-PET 阳性:一项多中心研究(摘要编号:85773)
演讲者杰玛-萨尔瓦多(瑞典)
- 临界值:特异性 90.0%、95.0%、97.5%。
- 调整年龄和 APOE 状态后的结果:
| p-tau217 only | Subsequent CSF amyloid-β 42/40 in patients positive for p-tau217 | |
|---|---|---|
| Positive predictive value | 72.9–81.2% | 90.8–95.3% ↑ |
| Negative predictive value | 82.5–86.2% | 82.8–86.7% |
| Accuracy | 82.4–83.8% | 84.0–87.3% ↑ |
| Overall rate of amyloid positivity | 10.9–18.1% | 9.3–14.3% ↓ |
| Probability of being assessed as positive on both p-tau217 and CSF | '- | 79.4–85.2% |
- “Salvadό说:”血浆p-tau217既可以作为独立的生物标记物,也可以作为CSF生物标记物之前的第一步(将其需求减少约80-90%),用于临床前AD临床试验的预筛选,具体取决于Aβ-PET阳性所需的确定性。
在记忆诊所环境中使用基于血液的阿尔茨海默病生物标记物面板来确定接受疾病调节治疗的资格:三种情况(摘要编号:91700)
演讲者: Sinthujah Vigneswaran(荷兰Sinthujah Vigneswaran(荷兰)
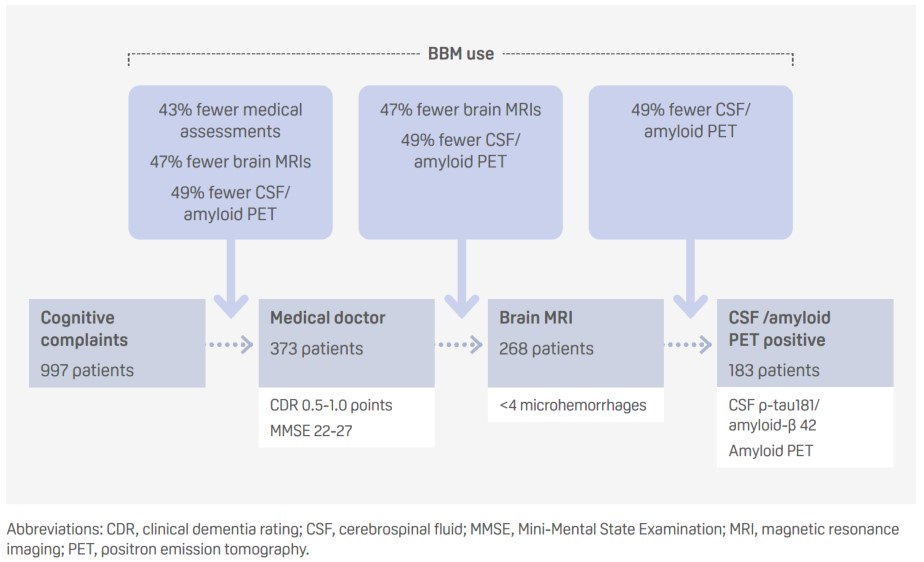
- 在标准诊断轨迹的不同阶段使用基于血液的生物标志物(BBMs)可以提高诊断过程的效率,无需进行额外检测,从而降低成本。
- p-tau217检测淀粉样蛋白阳性的尤登指数临界值特异性为92%,灵敏度为86%,特异性为87%,假阳性率和假阴性率分别为7%和32%。
评估血液生物标记物和淀粉样蛋白-PET在识别阿尔茨海默氏症病理患者方面的互换性(摘要编号:91465)
演讲者萨曼莎-伯纳姆(美国)
检测血浆生物标志物:
- PrecivityAD®结合了淀粉样蛋白-β42/40水平、APOE ε4和年龄。
- p-tau217.
血浆分层:
- 淀粉样蛋白-β42/40:无淀粉样蛋白斑块、有淀粉样蛋白斑块或介于两者之间。
- p-tau217:阴性、阳性或不确定。
排除 14.0% 的 PrecivityAD® 中期患者和 18.6% 的 p-tau217 中期患者后得出的结果:
| PrecivityAD® | p-tau217 | |
|---|---|---|
| Ruling in patients also amyloid PET visual read positive (PPV) | 86% | 88% |
| Ruling out patients also amyloid PET visual read negative (NPV) | 78% | 92% ↑ |
| Overall percentage agreement with amyloid PET visual read | 81% | 90% ↑ |
- 在选择淀粉样蛋白病变患者时,这两种基于血浆的生物标记物都达到了淀粉样蛋白 PET 的非劣效性标准,临界值为 37 centiloids (CL)。
- “Burnham说:”研究结果支持这样的假设,即血液生物标志物可与淀粉样蛋白-PET标准互换,用于选择适合接受新型淀粉样蛋白靶向疗法治疗并从中获益的患者。
阿尔茨海默病血液检测淀粉样蛋白-β 42/40、%p-tau217、181 和 205 比率以及 MTBR-243 在现实世界人群中的应用:SEABIRD 和 BioFINDER2 的结果(摘要编号:88405)
演讲者兰德尔-贝特曼(美国)
- 血浆微管结合区(MTBR)-tau243 对 tau-PET 阳性显示出良好的诊断准确性,并与晚期 Braak 区的 tau PET 有很强的相关性,这在淀粉样β阳性和非淀粉样β阳性患者中是一致的。
| All participants n=108 | Amyloid-β-positive participants n=51 | |
|---|---|---|
| MTBR-tau243 | 1.00 | 0.98 |
| p-tau217/tau217 ratio | 0.98 | 0.87 |
| p-tau217 concentration | 0.98 | 0.89 |
| All participants n=108 | Amyloid-β-positive participants n=51 | |
|---|---|---|
| Braak I–VI (Global) | 0.87 | 0.86 |
| Braak I–II | 0.89 | 0.54 |
| Braak III–IV | 0.89 | 0.79 |
| Braak V–VI | 0.85 | 0.86 |
AUC:接收者工作特征曲线下的面积
- 在所有患者(Rho=-0.82 vs -0.69)和有淀粉样蛋白斑块的患者(Rho=-0.54 vs -0.53)中,MTBR-tau243 与迷你精神状态检查(MMSE)评分的相关性与 tau PET 相似。
淀粉样蛋白病理学主要血液检测方法的正面对比评估(摘要编号:95506)
演讲者凯伦-彼得森(美国)
使用 AUC 分析预测血液生物标记物预测淀粉样蛋白-PET 阳性 (>20 CL) 的准确性的逻辑回归模型,并使用 DeLong 检验进行比较。
| Platform | Model | AUC |
|---|---|---|
| C2N Precivity™ | p-tau217 ratio* plus amyloid-β 42/40 | 0.929 ★ |
| p-tau217 ratio | 0.927 | |
| p-tau217 plus amyloid-β 42/40 | 0.921 | |
| p-tau217 | 0.916 | |
| amyloid-β 42/40 | 0.751 | |
| Fujirebio Lumipulse® | p-tau217 plus amyloid-β 42/40 | 0.911 |
| ptau217 | 0.896 | |
| amyloid-β 42/40 | 0.787 | |
| AlzPath Simoa® | p-tau217 | 0.885 |
| Janssen Simoa® | p-tau217 | 0.882 |
| Roche Elecsys® | p-tau181 plus amyloid-β 42/40 plus GFAP plus NfL | 0.677 to 0.873 |
| p-tau181 plus amyloid-β 42/40 plus NfL | 0.677 to 0.873 | |
| p-tau181 plus amyloid-β 42/40 | 0.677 to 0.873 | |
| p-tau181 | 0.677 to 0.873 | |
| amyloid-β 42/40 | 0.677 to 0.873 | |
| GFAP | 0.677 to 0.873 | |
| NfL | 0.677 to 0.873 | |
| Quanterix Simoa® | p-tau181 plus amyloid-β 42/40 plus GFAP plus NfL | 0.670 to 0.808 |
| p-tau181 plus amyloid-β 42/40 plus NfL | 0.670 to 0.808 | |
| p-tau181 plus amyloid-β 42/40 | 0.670 to 0.808 | |
| p-tau181 | 0.670 to 0.808 | |
| amyloid-β 42/40 | 0.670 to 0.808 | |
| GFAP | 0.670 to 0.808 | |
| NfL | 0.670 to 0.808 |
AUC:接收者操作特征曲线下的面积;GFAP:神经纤维酸性蛋白;NfL:神经丝光
*p-tau217 p-tau217 与非 tau217 的比率
血浆 p-tau217 和 tau-PET 预测认知功能未受损者未来认知能力下降的正面比较(摘要编号:90966)
演讲者:Rik Ossenkoppele(荷兰;瑞典Rik Ossenkoppele(荷兰;瑞典)
血浆 p-tau217 可预测迷你精神状态检查 (MMSE) 和改良的临床前阿尔茨海默氏症认知综合征 (mPACC) 的认知能力下降。
最佳预测模型:
- MMSE:血浆 p-tau217 加颞叶新皮层 tau-PET 摄取(neoT;测量时间相隔不到一年)。
- mPACC:血浆 p-tau217 和内侧颞叶 (MTL) 的 tau-PET 摄取量;测量时间相隔不到一年。
| Cognitive decline on MMSE | Cognitive decline on mPACC | |
|---|---|---|
| Plasma p-tau217 | R2 = 0.14 | R2 = 0.30 |
| MTL tau-PET | R2 = 0.17 | R2 = 0.32 |
| NeoT tau-PET | R2 = 0.21 | R2 = 0.31 |
用于阿尔茨海默病分期的血浆 Tau 生物标记物(摘要编号:88408)
演讲者Laia Montoliu-Gaya(瑞典)
- 根据对 BioFINDER-2 组群 553 例参与者血浆样本中六种磷酸化和六种非磷酸化 tau 肽(p-tau217、p-tau205、0N 中枢神经系统特异性和 tau 212-221)进行量化后得出的四种血浆 tau 肽阳性率,提出五步疾病分期模型。
- 该模型与淀粉样蛋白(A)和 tau(T)的 PET 状态以及早期内侧颞叶(MTL)和中期新颞叶(neoT)区域的 PET 阶段进行了比较。
| Plasma stage | A/T status | A- T- | A+ T- | A+ T+ | PET stage | MTL+ neoT– | MTL+ neoT+ | MTL+ neoT++ | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Plasma Stage | A/T Status | PET stage | ||||||||||||
| A- T- | A+ T- | A+ T- | MTL+ neoT- | MTL+ neoT+ | MTL+ neoT++ | |||||||||
| Stage 1: negative for all biomarkers | 80.8% | 19.2% | '- | '- | '- | '- | ||||||||
| Stage 2: p-tau217 positive | 3.4% | 40.9% | 55.7% | 22.6% | 22.6% | 31.0% | ||||||||
| Stage 3–4: p-tau217, p-tau205, and 0N CNS-specific positive | '- | '- | 100% | '- | 83.3-86.7% | |||||||||
| Stage 5: p-tau 217, p-tau205, 0N CNS- specific, and tau 212–221 positive | '- | '- | 100% | '- | '- | 100% | ||||||||
- “Montoliu-Gaya说:”我们的数据支持利用体液生物标志物对AD进行分期的观点。
利用血浆生物标记物预测阿尔茨海默病的淀粉样蛋白和 Tau 病理学阶段(摘要 ID:90581)
演讲者: Han-Kyeol Kim(大韩民国Han-Kyeol Kim(大韩民国)
血浆 p-tau217 与非 p-tau217 之比优于 p-tau217,淀粉样蛋白-β 42 与淀粉样蛋白-β 40 之比优于 PET 预测的 Thal 期和 Braak 期,尤其是在早期阶段。
血浆中 p-tau217 与非 p-tau217 比率的 AUC 值分别为
- 0.965 用于预测塔尔 I-II 阶段
- 0.848 用于预测塔尔阶段≥III
- 0.864 用于预测 Braak I-II
- 0.925 用于预测布拉克 III-IV
- 0.889 用于预测 Braak V-VI
阿尔茨海默病病理和神经变性的血液生物标志物的中晚期变化以及与脑淀粉样蛋白沉积的关系:ARIC-PET研究(摘要编号:91307)
演讲者普里亚-帕尔塔(美国)
血浆生物标志物在中年(平均年龄 58.5 岁)或晚年(平均年龄 76.2 岁)进行测量。
测试的生物标志物
- 淀粉样蛋白-β 42 与淀粉样蛋白-β 40 之比
- 磷酸化 (p)-tau181
- 神经丝光(NfL)
- 神经胶质纤维酸性蛋白(GFAP)
中年血浆生物标志物:中年时测量的生物标志物都不能预测晚年PET淀粉样蛋白阳性,即中位数19.3年后全球皮层标准化摄取值比值大于1.2。
晚期血浆生物标志物:晚年血浆生物标志物:在中位数 1.6 年前测量时,与晚年 PET 淀粉样蛋白阳性率有显著关联:
- 淀粉样蛋白-β 40/42 比率:几率比例=2.12
- P-TAU181:几率比=1.76
- GFAP:几率比=1.72
抗淀粉样蛋白疗法
主要启示
- 建议在 12 个月后对多那尼单抗进行限时给药,最好以 PET 扫描结果为阴性而非 tau 水平为指导。
- 包括生物标记物数据在内的证据支持尽早使用莱卡奈单抗,并在 3 年内持续获益。
TRAILBLAZER-ALZ 2(多那尼单抗)的启示:潜在的临床转化(发展中主题会议)
临床效率
演讲者詹妮弗-齐默(美国)
- 在76周时,多奈单抗将临床痴呆评级总分(CDR-GS,每3个月测量一次)中疾病进展到下一阶段阿尔茨海默病(AD)的风险大幅降低了37%。
- 在 76 周时,进展为中度 AD(CDR-GS 评分≥2 分)的患者比例大幅减少了 50%。
- 不同tau群体的疗效一致:中低tau和高tau患者的疾病进展风险分别显著降低了39%和38%。
- 包括西班牙裔/拉美裔参与者在内的不同亚群体的疗效一致。
可控的 ARIA 风险
演讲者亚历山德罗-比菲(美国)
- 服用多那尼单抗的患者中有 24% 出现淀粉样蛋白相关成像异常-水肿/渗出(ARIA-E),其中 18% 无症状,6% 有症状。
- 在接受多那尼单抗治疗的患者中,1.5% 的患者发生了严重的 ARIA-E 事件,其中 3 例(0.4%)患者死亡。
- 载脂蛋白(APO)E ε4同源基因携带者中的 ARIA-E 频率最高(40.6% 对非携带者的 15.7%)。
- 大多数患者只发作过一次 ARIA-E;68% 的患者重新服药,70% 的患者没有复发。
- ARIA-E的复发多为无症状、轻度至中度。
- 主要风险因素有
- APOE ε4 基因型。
- 基线微出血量。
- 基线时存在皮质浅层鳞状上皮细胞增多症。
- 风险管理建议:
- 在治疗前识别高风险患者。
- 坚持磁共振成像监测计划。
- 根据需要调整、中断或中止治疗。
- 对严重或有症状的 ARIA 使用皮质类固醇。
限时用药
演讲者艾米丽-柯林斯(美国)
- 在符合剂量完成标准的患者中,淀粉样蛋白水平仍然很低,重新累积率为 2.8 centiloids (CL)/年。
- 转用安慰剂的平均时间为 47 周,此后治疗组之间的差异继续扩大。
- 三分之二的患者在12个月时淀粉样蛋白PET水平低于24.1CL,这与PET扫描的肉眼阴性结果一致,可用于帮助确定何时停止治疗。
- 较低的基线淀粉样蛋白水平预示着淀粉样蛋白 PET 能更早地降低到 24.1 CL 以下。
- 血浆p-tau不足以准确判断多奈单抗淀粉样蛋白的清除情况,因为淀粉样蛋白清除后,血浆p-tau仍能反映tau的病理变化。
是否有证据表明利卡单抗长期治疗可持续获益?从长期疗效、安全性和生物标志物数据中得出的收益/风险更新(摘要编号:92094)
演讲者克里斯托弗-范戴克(美国)
莱卡奈单抗治疗效果持续 3 年的证据:
- 36 个月时,临床痴呆评级-方框总和(CDR-SB)与基线相比的平均变化为 3.09 分,而 18 个月时的平均变化为 1.20 分。
- 与ADNI研究中的匹配历史对照组相比,CDR-SB的差异达到了0.95分,与安慰剂相比,18个月时的差异增加了0.45分,疾病进展到下一阶段的风险降低了30%。
低 tau 和淀粉样蛋白组表现尤为出色,支持尽早使用 lecanemab:
- 在基线无 tau PET 或低 tau PET(SUVR <1.06)的 58 名患者中,59% 的患者在 36 个月时 CDR-SB 评分没有下降,51% 的患者有所改善。
- 在基线淀粉样蛋白PET较低(<60 CL)的151名患者中,46%的患者CDR-SB评分没有下降,33%的患者评分有所提高。
血浆生物标记物数据支持继续使用莱卡奈单抗:
- 开始使用莱卡奈单抗 18 个月的患者在 3 个月内淀粉样蛋白 PET 和血浆淀粉样蛋白-β 42/40 比率有所改善。
- 尽管约 70% 的患者在 18 个月时淀粉样蛋白阴性(<30 CL),但在 18 个月至 36 个月期间仍能继续获得治疗益处。
- 在莱卡奈单抗治疗的前 18 个月,血浆中 p-tau217 的水平会下降,但服用安慰剂后会上升。
- 与安慰剂相比,莱卡奈单抗治疗18个月后,CSF MTBR-tau243下降了44%。
长期 ARIA 风险低
- 在核心研究和扩展阶段,使用莱卡奈单抗后,淀粉样蛋白相关成像异常-水肿/渗出(ARIA-E)的暴露调整率为每100人年6.8例,而仅在核心研究中为每100人年9.6例。
- ARIA-E 主要发生在治疗的前 6 个月,之后就很少发生了,发生率与安慰剂相似。
- ARIA 与长期进展加速无关。
最新临床药理数据和模型如何支持持续使用来卡尼单抗?(摘要编号:92091)
演讲者拉丽莎-雷德曼(美国)
研究 201: 31 名早期阿尔茨海默病患者在接受 18 个月的治疗后停止服用 lecanemab(10 毫克/千克,每 2 周一次),平均 2 年后再继续服用。
- lecanemab的双重作用意味着它不仅能清除斑块,还能靶向毒性很强的原纤维,这些原纤维在淀粉样蛋白被清除后会继续形成并导致阿尔茨海默病的病理变化。
在 201 号研究中,中断莱卡奈单抗的治疗导致:
- 淀粉样蛋白 PET 的再积累率为 21%。
- 淀粉样蛋白-β 42/40 比率恶化 47%。
- 神经胶质纤维酸性蛋白(GFAP)30% 的再积累。
- 24% 的 p-tau181 再积累。
- 13% 的 p-tau217 再积累。
药代动力学和药效学模型显示,莱卡奈单抗的治疗效果会减半:
- 6 个月后,淀粉样蛋白-β 42/40 比率。
- 淀粉样蛋白 PET 为 12.1 年以内。
- p-tau181 为 1.6 年。
- 1.7年后为GFAP。
在18个月或24个月时开始每月服用10毫克/千克的莱卡奈单抗维持剂量,足以防止淀粉样蛋白的再次积累和血浆生物标志物的恶化。
- 就淀粉样蛋白 PET 和 CDR-SB 测量的临床结果而言,其效果与每两周给药 4 年的效果相当。
点击下面的链接下载 Microdigest 2 pdf:
下载 Microdigest 2 中文版 PDF您还可以从 AD/PD & CONy 下载 Microdigest:
下载 Microdigest 1 中文版 PDF





