マイクロダイジェスト 3
CTADラウンドアップ
ここでは、新規バイオマーカーと抗アミロイド療法に焦点を当て、CTAD 2024で発表された主要データを要約する。

臨床試験のスクリーニング
主な収穫
- p-tau217比は、すべての人種および民族集団において、アミロイドβ陽電子放射断層撮影(PET)スクリーニングの失敗率を減少させるための適切なバイオマーカーである。
- 血漿適合率が低いということは、人種的・民族的にアミロイド異常の有病率に差があることを示唆しており、抗アミロイド治療試験への参加率が低い一因となっている。
- タウPETは認知機能と強く相関する優れたエンドポイントである。
AHEAD 3-45試験:AD前臨床試験における新規スクリーニングプロセスのデザインと結果(抄録:LBS1)
AHEAD 3-45試験は、2つの姉妹試験から構成されている:
- A3試験は、アミロイドβPETが中等度(20-40センチロイド[CL] )の認知機能非障害者を対象に、レカネマブ静注(5mg/kg漸増後、10mg/kgを毎月208週間投与)とプラセボを比較する第2相4年間試験である。目的は、4年間の認知機能低下(Preclinical Alzheimer’s Cognitive Composite 5[PACC-5] )を予防することである。
- A45試験は、アミロイドβPET陽性(40CL以上)で認知機能に障害のない人を対象に、レカネマブ静注(5mg/kg隔週6週間、その後10mg/kg隔週86週間、その後月1回120週間)とプラセボを比較する第3相4年試験である。目的は、アミロイドβの蓄積を遅らせることである(アミロイドPETおよびタウPET)。
審査期間は終了したばかりだ。
AHEAD 3-45 試験における血漿バイオマーカー、アミロイドおよびタウ PET イメージングのスクリーニング(発表 2)
発表者:レイサ・スパーリング(米国)
- A3およびA45の審査プロセス:
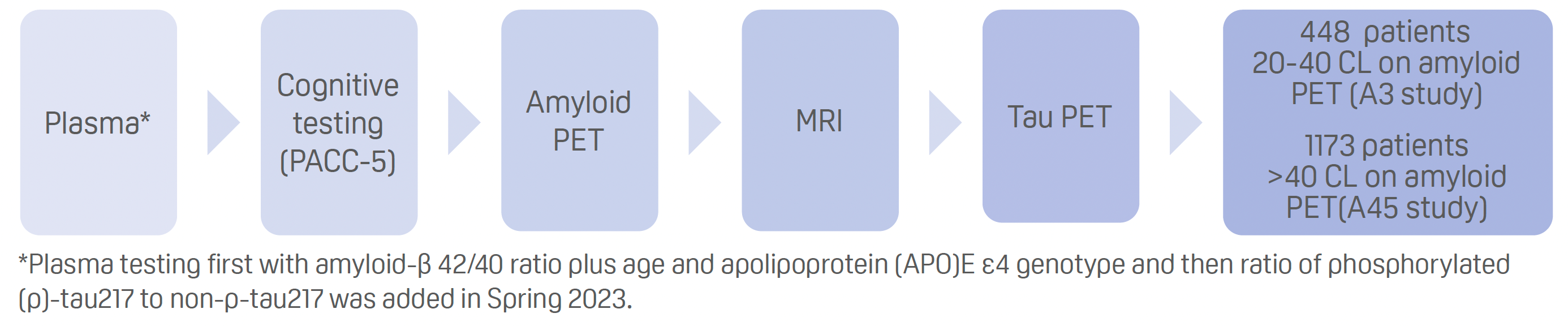
結果
- アミロイド-β42/40比の血漿検査を含めると、11回以上のCLを予測するアミロイドPETの失敗率が約75%から約55%に減少した。
- p-tau217比の追加により、18CL以上のアミロイドPETによる予測不能率はさらに低下し、約40-45%となった。
- 血漿p-tau217比は、20CL以上のアミロイドPETにおいて0.95の受信者動作特性曲線下面積を達成した。
- 完全血漿検査モデルによる血漿検査では、40以上のCLを予測するアミロイドPETの失敗率は25%に減少した。
- 内側側頭葉と大脳新皮質のタウPETは、A3試験参加者よりもA45試験参加者の方が高かった。
- タウPETはPACC-5で認知機能と最も強い相関を示した。
「p-tau217比の早期上昇は、将来のアミロイド陽性を予防することを目的とした、より早期の介入試験に有用であることが証明されるかもしれません 。 「この結果は、タウPETを重要なエンドポイントとして支持するものであり、A3とA45における画像、バイオマーカー、認知機能の橋渡しとなる可能性がある。
前臨床AD試験における血漿p-tau217バイオマーカー適格率における人種・民族差(発表3)
プレゼンタードリス・モリーナ・ヘンリー
- p-tau217比が追加されたウインドウにおける血漿バイオマーカーアルゴリズムの能力を理解することで、人種や民族の異なる不特定集団における18CL以上のアミロイドPET適格性を検出することができる。
結果
- ヒスパニック系でない白人の成人と比較して、すべての人種的・民族的弱者グループの血漿適合率が低い。
- 血漿適格者におけるPET適格率は、人種・民族の違いによる差はなく、同程度であった。
| 人種/民族グループ | 人数 | 血漿適合率 | 血漿適格患者のうちPET適格患者の割合 |
|---|---|---|---|
| 非ヒスパニック系白人 | 4832 | 27% | 71% |
| ヒスパニック 白人 | 877 | 19% | 63% |
| ヒスパニック 黒人 | 62 | 11% | 75% |
| 非ヒスパニック系 アジア人 | 155 | 15% | 50% |
| 非ヒスパニック系黒人 | 511 | 19% | 68% |
「血漿中の適合率が低いことは、これらのグループにおけるアミロイド異常の有病率に差があることを示唆している。
「PETの適格性はどのグループでも同じであり、同じ血漿予測アルゴリズムが人種や民族を超えて適切に適用されたことを裏付けています」と 彼女は付け加えた。
「このことは、アミロイド有病率が低い人種的・民族的劣等集団の人々における認知症リスクの高さを、他の要因が説明している可能性を示唆している。
バイオマーカーとAD診断
主な収穫
- β-シヌクレインは、アルツハイマー病(AD)における新しいシナプス血液ベースのバイオマーカーになるかもしれない。
- 臨床的認知症評価尺度(Clinical Dementia Rating Scale-Sum of Boxes)の0.5単位ごとに費やされた時間は、治療効果を評価するのに役立つであろう。
- 多項目の血液バイオマーカー検査は、診断の意思決定に役立つかもしれない。
- アミロイド陽電子放射断層撮影(PET)陽性率と診断時の臨床病期における人種的/民族的格差は、治療へのアクセスを改善するために対処する必要がある。
- 慢性腎臓病のような併存疾患との関連において、p-tau217のパフォーマンスを容易に解釈するための戦略を開発する必要がある。
- 血液ベースのバイオマーカーのさまざまな役割は、ADの段階的診断アプローチへの道を開く可能性がある。
- 抗アミロイド療法を推奨する前に、アミロイドβ陽性について脳脊髄液(CSF)とPETの測定値が異なる場合には、さらなる検査が推奨される。
常染色体優性アルツハイマー病の無症候性患者におけるシナプス血中マーカーβシヌクレインの早期増加 常染色体優性アルツハイマー病(抄録ID OC14)
プレゼンターパトリック・オークル(ドイツ)
- 免疫沈降質量分析法を用いて、Dominantly Inherited Alzheimer Network(DIAN)研究の参加者178人の血液サンプル中のシナプス前タンパク質β-シヌクレインを定量した。
- 31人の症候性変異キャリア、78人の無症候性変異キャリア、69人の認知機能に障害のない変異非キャリアを含む。
結果
- β-シヌクレイン濃度は、常染色体優性ADの無症候性患者では認知機能に障害のない人に比べて有意に高く、症状のある患者では最も高かった。
- 血中β-シヌクレイン濃度は、症状発現の約11年前から変異保有者で上昇し始めた。
- 体液中のバイオマーカー濃度が、突然変異の保因者と非保因者の間で有意に乖離した時期に従って、早い時期から順にランキング:
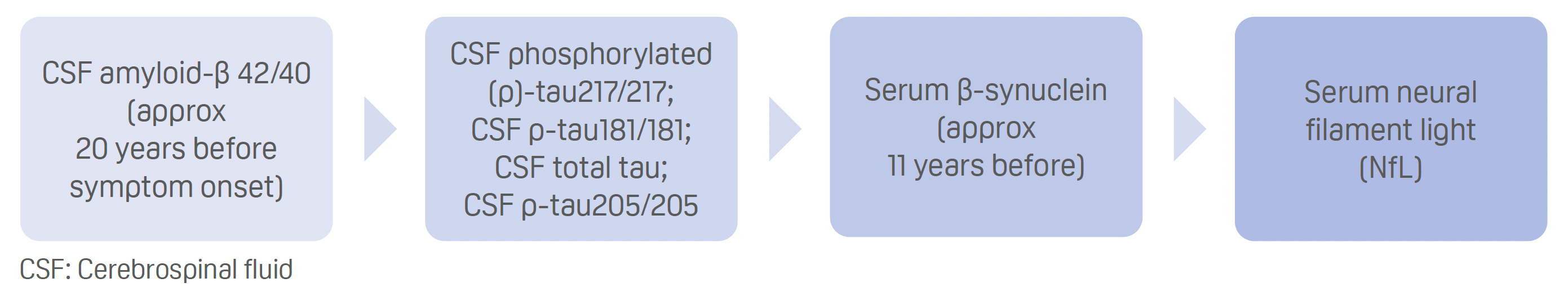
- 血清β-シヌクレインの軌跡は、認知障害、脳萎縮、代謝低下の画像的測定に先行する。
- 血清βシヌクレインはアミロイドβ陽性を予測する能力が中程度であった(受信者動作特性曲線下面積0.75)。
- 血清β-シヌクレインは認知障害と有意な相関があった。
血液中のβ-シヌクレインは、「診断、予後、[and] 、薬剤開発のためのシナプスマーカーとして簡単に利用できる」可能性がある 、とOeckl氏は述べた。
CDR-SBにおける臨床経過:DIANとADNIのコホートにおける各レベルでの滞留時間(抄録番号OC19)
発表者グオチャオ・ワン(米国)
- DIAN(常染色体優性AD)とADNI(散発性AD)の2つのコホートにおいて、0.5単位のClinical Dementia Rating Scale-Sum of Boxes(CDR-SB)が次のレベルに進むまでに費やす時間の長さ(滞留時間)を、疾患進行のランダム効果モデルを用いて検討した。
結果
- 常染色体優性AD:CDR-SBが3点以上の場合、0.5単位CDR-SBあたりの滞在期間は0.5年以下。
- 散発的なAD:CDR-SBが3.5ポイント以上の場合、0.5単位CDR-SBあたりの滞在期間が0.5年以下。
- CDR-SBスコアが0.5点から3.5点になるまでの期間:常染色体優性ADでは平均6.5年、散発性ADでは5.6年で、その差は約0.9年であった。
滞留時間を用いれば、例えばレカネマブのクラリティAD試験のオープンラベル延長相の患者について治療効果を計算することができる:
- ベースラインのCDR-SBスコア3.17点から、プラセボ投与群では3.09点低下するのに2.3年、レカネマブ投与群では3.0年かかり、0.7年病勢進行が遅れると推定された。
CDR-SBにおける各0.5単位レベルの滞留時間は、「治療効果を解釈し評価するための標準化された別の方法を提供することができる」と王氏は述べた。
脳アミロイド上昇のCSFとPETによる判定の不一致とその予後的意義(抄録:LB10)
プレゼンターデイビッド・ノップマン(米国)
- 軽度認知障害を有するADNIコホート参加者587人を対象に、アミロイドβ陽性のCSF測定とPET測定の不一致に伴う認知機能低下を評価した。
結果
- 検査結果が一致しないことはまれで、その割合は約5%であった。
- CSFアミロイドとPETアミロイドの両方で陰性と判定された患者と、どちらか一方で陰性と判定された不一致の患者は、ベースライン時の認知機能はほぼ同じであり、両測定で陽性と判定された患者と比較して認知機能は良好であった。
- 髄液アミロイドが陽性でPETアミロイドが陽性でなかった患者では、髄液のp-tau/アミロイドβ比は両測定で陽性であった患者よりもかなり低かった。
- 中央値で4年間追跡した結果、検査結果が不一致であった患者では、両検査で陽性であった患者とは異なり、Rey auditory Verbal Learning Test Sumum of Trials 1-6またはClinical Dementia Rating Scale-Sum of Boxesのスコアが有意に低下することはなかった。
- 追跡期間中の認知症発症率は、両測定で陽性と判定された患者においてのみ有意に上昇した(100人年当たり17.3人)が、陰性または両測定で不一致と判定された患者では同程度であった(100人年当たり1.9〜3.0人)。
「MCIのCSF陽性/PET陰性パターンを持つ患者は、グループごとの減少を示さなかったので、抗アミロイドモノクローナル抗体治療を勧める前に、疾患進行の可能性に関する追加的なエビデンスを得る必要があります」とKnopman氏は述べた。
認知機能障害評価のための多項目血中バイオマーカー検査の影響評価:QUIP II臨床有用性試験の結果(抄録番号OC32)
プレゼンタージョエル・ブラウンシュタイン(米国)
- 203名の認知障害患者を治療する12名の臨床医を対象に、臨床管理および意思決定におけるPrecivityAD2(C2N Diagnostics社、米国ミズーリ州セントルイス)の使用を評価するための調査を行った。
- この血液検査では、血漿中のアミロイドβ42、40、p-tau217、非p-tau217の濃度を数値化し、アミロイド陽性確率スコア(APS)2として0~100点満点で表示する。
結果
- 患者の51%が陰性であった。
- 使用目的との一致率99%。
- AD診断の確実性、薬物療法、さらなる脳アミロイド評価において75%の変化。
- APS2の結果と臨床医が報告したADの可能性との間には、血液検査を行う前は弱い相関があり、血液検査を行った後は強い相関があった。
- 陰性患者の場合、臨床医が報告したAD確率は、血液検査使用前の53%から11%に減少し、陽性患者では65%から93%に増加した。
- 血液検査使用前と使用後では、陰性患者ではAD治療薬の処方が有意に減少し、陽性患者では有意に増加した。
- 追加の脳アミロイド検査は、陰性患者で70%、陽性患者で26%減少した。
「PrecivityAD2™血液検査は、AD診断の確実性、薬物療法の管理、認知機能障害を評価された患者におけるアミロイドの追加評価などの意思決定において、臨床的に意味のある変化をもたらしたと確信しています」と Braunstein氏は述べた。
プレゼンターギル・ラビノビッチ(米国)
アミロイドPETの結果と健康の社会的決定要因の人種/民族による差異:New IDEASの結果(抄録OC08)
- 軽度認知障害(MCI;64%)または認知症(37%)を有する4845人のNew IDEAS参加者のアミロイドPET陽性率、臨床病期、健康の社会的決定要因を比較したところ、そのうち21%が黒人/アフリカ系アメリカ人(BAA)、18%がラテン系/ヒスパニック系(LAT)、61%がその他の人種または民族(NBL)と自認した。
結果
BAAとLAのグループは
- アミロイドPET陽性率はNBL群より28%低く、それぞれ60.7%、60.8%対68.2%であった;
- 高血圧(73.3%、61.5%対54.3%)、糖尿病(29.9%、29.8%対16.3%)などの血管合併症を有する傾向がより強かった;
- NBL群に比べ、MCIに比して認知症を呈する割合が高く、47.4%、43.5%対30.5%であった;
- は非典型的な症状を示すことが多く、診断が困難であった(36.0%、35.55対26.6%);
- ベースライン時の平均ミニメンタルステート検査得点は、NBL群より低かった(21点、21点対25点)。
「こうした修正可能な格差に対処することは、ケアへのアクセスや認知症予防戦略の実施における公平性を高めるために非常に重要です」と ラビノビッチ氏は語った。
アフリカ系アメリカ人コホートにおける血漿p-tau217の性能:中年期アルツハイマー病と闘うアフリカ系アメリカ人研究からの知見(抄録:OC13)
プレゼンタージルダ・アニス(米国)
- AA-FAIMコホートの非ヒスパニック系黒人またはアフリカ系アメリカ人であり、腎機能障害、心血管疾患、高血圧、糖尿病、肥満のうち少なくとも1つを併存する233人の認知機能障害のない成人を対象に、アミロイドPET陽性を検出する血漿p-tau217の精度を評価した。
結果
- 血漿p-tau217の高値は、軽度(推算糸球体濾過量[eGFR] 1.73m2あたり90mL/分未満)および中等度から重度(eGFR 1.73m2あたり60mL/分未満)の腎機能障害、ならびに心血管系疾患(心筋梗塞、脳卒中、うっ血性心不全)と有意に関連していた。
- それぞれ38人と64人の小サブサンプルでは、どちらの関連もアミロイド負荷では説明できなかった。
- 血漿p-tau217レベルは、年齢と性別をコントロールした後では、ステージ1または2の高血圧、糖尿病、肥満のある患者では有意な増加はみられなかった。
- AA-FAIMコホートからの65人の患者におけるアミロイドPET陽性を検出するための血漿p-tau217の精度は、0.35pg/mLのカットオフ点で90%であり、感度は94%、特異度は80%であった(ADに関するグローバルCEOイニシアチブは、血液ベースのバイオマーカーのプライマリケアでの使用について、それぞれ90%および85%を推奨している)。
「血漿p-tau217の正確な解釈を容易にするための戦略を検討する必要があります。
ステップワイズバイオマーカーガイド診断におけるアルツハイマー病血漿バイオマーカーの役割の違い:アジア人集団での比較(抄録:OC38)
プレゼンターシン・デウン(韓国)
- アジア人2984人(認知機能障害なし22%、AD認知機能障害68%、皮質下血管性認知機能障害6%、前頭側頭型認知症3%)を対象に、血漿マーカーの役割の違いを検討し、バイオマーカーによるAD診断をより効率的に行うための段階的な戦略の一部として使用できるかどうかを検討した。
- 血漿バイオマーカー:アミロイドβ42/40;p-tau181;p-tau217;p-tau231;GFAP;NfL。
結果
| 最良のバイオマーカー | 役割 | AUC |
|---|---|---|
| NfL | 認知障害のある患者とない患者を識別 | 0.71–0.94 |
| p-tau217 | 全群でアミロイドβPET陽性を識別 | 0.88–0.95 |
| p-tau217 | AD認知障害患者におけるタウPET陽性を識別 | 0.90–0.91 |
| p-tau217 | アミロイドβPET陽性のAD認知障害患者とアミロイドβPET陰性の非AD認知障害患者を識別 | 0.94–0.95 |
| p-tau217とGFAP | Predicted cognitive decline in cognitively unimpaired patients | 該当なし |
AUC:受信者動作特性曲線下面積;N/A:該当なし;NfL:ニューロフィラメントライト;p:リン酸化;PET:陽電子放射断層撮影;GFAP:グリア線維酸性タンパク質
「これらの知見は、段階的診断アプローチにおけるアルツハイマー病血漿バイオマーカーの役割の違いの重要性を強調するものです」。 とShin研究員は述べた。
抗アミロイド療法
主な収穫
- ドナネマブについては、適切な治療候補者を特定するための適正使用勧告が出されている。
- 抗アミロイド療法の適応は比較的低く、血液ベースのバイオマーカーを含むより広範なスクリーニングによって改善される可能性がある。
- 現実の患者は適切に選択され、FDAが承認した添付文書情報に従ってレカネマブの投与を受けている。
- レカネマブは臨床において患者の忍容性が高く、アドヒアランスも良好である。
ドナネマブ:適切な使用に関する推奨事項(抄録:LB01)
プレゼンターギル・ラビノビッチ(米国)
- 本勧告は、ドナネマブの臨床試験データ、FDA処方情報、その他の関連文献、専門家の意見に基づき、ADおよび関連疾患治療ワークグループにより作成された。
結果
ドナネマブ治療の対象となる患者は、以下の条件を満たしていなければならない:
- 軽度認知障害(MCI)またはADによる軽度認知症:Global Deterioration Scaleの臨床病期が3~4期で、Mini-Mental State Examination(MMSE)のスコアが20~30点。
- 脳脊髄液(CSF)バイオマーカー(アミロイドβ42/40またはリン酸化(p)-タウ181/アミロイドβ42比)または陽電子放射断層撮影(PET)によりアミロイドβ病理の証拠を確認。
- 治療前に行われたアポリポ蛋白(アポ)E遺伝子型判定と磁気共鳴画像法(MRI)。
ドナネマブ治療の対象とはならない:
- 4個以上の微小出血、1cm以上の大出血、表在性シデローシスなど、重度の白質病変または重大な脳アミロイド血管症をMRIで示す患者。
- 抗凝固薬を服用している患者。
さらなる提言
- ドナネマブ治療中は血栓溶解薬を使用すべきではない;機械的血栓除去術は可能である。
- MRIで大出血、1カ所以上の表在性シデローシス、10カ所以上の微小出血、2回以上のアミロイド関連画像異常(ARIA)、または重度のARIAが認められた場合、ドナネマブの投与を中止する。
- アミロイドPETが陰性であれば、12~18ヵ月後に治療の中止を検討する。
ラビノビッチ氏は、これらは 「推奨であり、ガイドラインや基準ではない。
実世界のメモリークリニック集団における抗アミロイド治療の適格性(抄録:OC22)
プレゼンターアンナ・マトン(スウェーデン)
- レカネマブの適切な使用に関する推奨を、スウェーデンの7つのメモリークリニックから得られた2126人の代表的な実際の患者サンプルに適用し、誰が抗アミロイド療法の対象となるかを調べた。
結果
- 平均年齢77.1歳、女性50.4%。
- 平均MMSEは27点であった。
- 患者の32%が病理学的Fazekasスコアを有していた。
- 62%がMCI、24%がAD認知症であった。
- 患者の17%が抗凝固薬を、17%が抗血小板薬を服用していた。
- CSFバイオマーカーの測定が可能な918人の患者のうち、34.3%にアミロイドβ42の異常、32.5%にリン酸化(p)タウの異常、50.4%に総タウの異常、20.6%にニューロフィラメント光の異常が認められた。
- 774例のATNプロファイルは以下の通りであった:
| A-T-N- | A–T–N+ | A+T–N+ | A–T+N– | A+T–N– | A–T+N+ | A+T+N– | A+T+N+ |
|---|---|---|---|---|---|---|---|
| 26.1% | 18.5% | 11.8% | 10.7% | 9.6% | 9.3% | 7.0% | 7.1% |
A:CSFアミロイドβ42、T:CSF p-tau181、N:内側側頭葉萎縮 ハイライトされたプロファイルは、抗アミロイド治療の対象となったものである。
- 推奨された除外基準に基づくと、86人が抗アミロイド療法の対象となったが、これはCSF対象患者の9.4%、全患者の4.1%であった。
- これらの患者はMCI患者の10%(合計64%)、AD認知症患者の25%(合計36%)であった。
「全体として、対象となりうる患者の割合は比較的低いでしょう 。「ADの血液バイオマーカーを含む、より広範なスクリーニングアプローチによって、潜在的な患者数は増加する可能性がある。
臨床におけるレカネマブの使用に関する1年間の経験(抄録:LBS2) 米国における実環境でのレカネマブ治療(発表1)
プレゼンターマルワン・サッバーグ
- レカネマブ治療を開始し(主に2023年10月以降)、平均追跡期間が129日で、治療開始12カ月前の臨床活動に関する情報を有していた患者3155人について、Komodo研究データベースからデータを評価した。
結果
- 患者の平均年齢は75歳、84.3%が白人、93.3%が都市部出身、55.8%が女性であった。
- 大多数が併存疾患を有しており、主なものは脂質異常症(54.4%)と高血圧(45.7%)であった。
- 60.8%がMCI、83.8%がADであった。
- 67.6%が経口抗AD薬(アセチルコリンエステラーゼ阻害薬またはメマンチン)を、3.7%が抗凝固薬を、4.1%が抗血小板を服用していた。
- 診断から治療開始までの平均期間は4.9ヵ月であった。
- 患者は毎月2回の点滴を平均16.5日以内に受け、最初のMRI検査は治療開始から平均46.7日後に行われた。
- アドヒアランス(2回の点滴の間隔が90日以内であること)は85.1%であった。
Sabbagh氏によれば、患者はレカネマブを“ラベル通り、時間通りに ” 投与されていた。彼らは“治療と不治療の結果を理解すれば、レカネマブの投与を継続することに非常に意欲的である”。
ある大学医療センターにおけるレカネマブの臨床使用(発表2)
プレゼンターローレンス・ホーニグ
- 米国ニューヨークのアーバイン医療センターにおけるレカネマブによる162例の治療経験。
結果
- 患者の平均年齢は73歳、90%が白人、56%が女性であった。
- 併存疾患は多く、脳卒中や出血が2%、血管奇形が3%であった。
- MCIまたはAD認知症の証拠は、86%がCSFバイオマーカーで、26%がPETで、12%が両方で確認された。
- 患者の2%がペースメーカーを、1%が抗凝固剤を服用していた。
- MMSEの平均点は23.6点で、11点から30点の範囲であった。
- ApoE遺伝子型判定は89%に実施されたが、残りの11%は実施されなかった。
- 全患者とリスクディスカッションを行い、治療前のMRIで微小出血が4つ以上あった患者のみを除外した。
- 18ヵ月間に平均13.1回の注入が行われ、治療後に最大4回のMRI検査が行われた。
- ARIAが疑われたため、予定外のMRI検査が9回実施され、うち1回は陽性であった。
- ARIA浮腫・滲出(ARIA-E)の発生率は11%、ARIA微小出血(ARIA-H)の発生率は5%であった。
- ARIA-Eは通常早期に発現し、ほとんどが無症状で、レカネマブの投与を再開すると数ヵ月で消失した。
- 治療を中断した患者は9%で、主にARIA-Eが原因であった。
- ARIA-Eの17例中16例は無症状であった。
- 治療を中止した患者は8%で、ARIA-Eで1人、ARIA-Hで2人、ARIA-EとARIA-Hの両方で1人がその後死亡し、負担、無関心、保険の問題、有益性の欠如のために8人、転居のために追跡不能になった4人であった。
レカネマブの臨床経験は 、「臨床試験と似て非なるものでした 。レカネマブは “安全で管理しやすく” 、“患者に広く受け入れられ、コンプライアンスも良かった”。
ARIA
主な収穫
- ドナネマブの用量漸増は、ARIA-E率を低下させるのに役立つ可能性がある。
- 抗アミロイド治療薬のアミロイドプラークではなく脳アミロイド血管症への “標的外 “結合は、ARIA-E発症率の違いを説明しないかもしれない。
- AIは、臨床医にとって有害事象のコーディングをより効率的にするのに役立つだろう。
- 超高速MRIのばらつきは標準的なスキャンと変わらない。
成人早期症候性アルツハイマー病患者におけるドナネマブ投与レジメンの違いによるARIA-Eおよびアミロイド低下への影響:TRAILBLAZER-ALZ 6の主要評価結果(抄録番号:OC01)
プレゼンタージョン・シムズ(米国)
- 第3b相試験では、AD患者843人を対象に、ドナネマブの投与レジメンを変更することでARIA-E発生率を低下させることができるかどうかを検討した。
–
–
標準的漸増-最初の3回は700mg、4回目は1,400mgのドナネマブを4週間ごとに点滴静注。
修正漸増レジメン-ドナネマブ点滴静注:1回目350mg、2回目700mg、3回目1050mg、4回目1400mg。
結果
- 24週目までのARIA-E発現率は、標準的漸増群13.7%に対し、変更漸増群23.7%と、変更漸増群の方が有意に低かった。
- 変更された滴定により、ARIA-E率が少なくとも20%低下する確率は94%であり、80%以上という主要試験目的を達成した。
- 24週時点のMRIでは、標準的漸増群では76%であったのに対し、修正漸増群では86%の患者にARIA-Eが認められなかった。
- その他の重篤な有害事象、治療中止、治療関連有害事象については、2つの漸増レジメン間に差はなかった。
- 修正漸増群のARIA-E投与中の患者で、脳実質内出血による死亡が1例あった
- アミロイド低下作用は、修正漸増レジメンと標準漸増レジメンで同等であった(ベースラインからの平均減少量はそれぞれ56.3および58.8センチロイド)。
この結果は、「十分なアミロイド減少を維持しながら、漸増的アプローチによりARIAリスクを抑制できる可能性がある」ことを示唆している。
血管内Aβ凝集体に対する抗アミロイド抗体の選好性は、ARIAの発生率を説明しない(抄録:OC35)
プレゼンターアンドリュー・スターン
- アミロイド関連画像異常の浮腫および/または滲出液(ARIA-E)発生率が各治療薬で異なることの説明として、アデュカヌマブ、ドナネマブ、レカネマブが、「オンターゲット」アミロイドに対して「オフターゲット」脳アミロイド血管症に結合する親和性を検証した。
結果
- 過去に報告されたARIA-Eレート:
- アデュカヌマブは35.2%(*2.8倍の差)
- 24.0%(ドナネマブ
- レカネマブで12.6%(*2.8倍の差)

- アミノ酸配列から合成された抗体は、CAAに富む髄膜アミロイドβ40とプラークに富む実質アミロイドβ42に優先的に結合することが平均して増加した:
- アデュカヌマブで1.51倍
- ドナネマブで1.63倍
- レカネマブで1.85倍
- 3つの治療法の間に有意差はなく、アデュカヌマブによる0.83~1.8倍の優先的結合は、レカネマブと比較したARIA-E率の2.8倍の差を説明するものではない。
Stern氏は、「髄膜アミロイドβ40に富んだ凝集体に対する抗体の選好性は、実質アミロイドβ42に富んだ凝集体に対するものであり、ARIA率の違いを説明することはできない」と結論づけた。
アルツハイマー病臨床試験における人工知能を活用した安全性モニタリング(抄録:OC36)
プレゼンターグスタボ・ヒメネス=マジオラ(米国)
- 症状のあるAD患者を対象とした8つの臨床試験から収集したデータを用いて、臨床医による980件の有害事象のコーディングを補強するための自然言語処理と人工知能(AI)の使用を評価した。
結果
- AIは、全体的(正確度88%対71%)およびコード頻度範囲にわたって従来の臨床医ベースのコーディングを上回り、報告レベル(専門家による臨床レビューおよび生物統計学的分析後)では3~13%正確度が向上した。
- AIによるコーディングは、AD前の患者を対象とした別のコホート(A4研究)において、臨床医によるコーディングと同程度の約70%であったが、報告レベルでの精度は3~5%向上した。
- AIを用いたAEコーディングはコスト効率が高く、約80%のコスト削減を実現した。
「人工知能に基づくコーディングは、臨床医によるコーディングと比較して精度を落とすことなく瞬時に行うことができ、コストを削減し、安全性データの可用性を向上させることが できます」とJimenez-Maggiora氏は述べた。
アルツハイマー病の診断と治療に役立つ超高速MRIプロトコル(抄録:OC34)
プレゼンターミゲル・ロサ=グリロ(英国)
- 90人を対象に、3人の神経内科医が波動制御高度平行画像を用いた高速画像スキャンを解釈する際のばらつきを、標準的な臨床磁気共鳴画像(MRI)スキャンと比較した(高速スキャンと標準スキャン):41.1%は神経変性脳疾患なし、21.1%はAD、12.2%は前頭側頭葉変性症(FTLD)、8.9%は血管性認知障害(VCI)、16.7%はその他の診断であった。
結果
- 高速スキャンにより、標準スキャンに比べて撮影時間を約63%短縮(6分29秒 vs 17分39秒)
- 高速スキャンによってもたらされた変動は標準スキャンよりも小さく、2つの方法の非劣性を示す証拠となった。
評価者間信頼性カッパ係数*は以下の通り:
- 正常:高速スキャン=0.61、標準スキャン=0.65、スキャン間:0.80
- AD:高速スキャン=0.38、標準スキャン=0.42、スキャン間=0.72
- FTLD:高速スキャン=0.79、標準スキャン=0.71、スキャン間=0.95
- VCI:高速スキャン=0.75、標準スキャン=0.75、スキャン間=0.95
- その他の診断高速スキャン=0.48、標準スキャン=0.50、スキャン間=0.76
* 0.21~0.40=まあまあ、0.41~0.60=中程度、0.61~0.80=かなり
「現場での実際の時間短縮や、異なる現場強度での超高速実装を評価するためには、さらなる研究が必要です」と ロサ-グリロは言う。
CTADからマイクロダイジェスト3のPDFをダウンロードするには、以下をクリックしてください:
マイクロダイジェスト3 JP PDFをダウンロードAAICからマイクロダイジェスト2のPDFをダウンロードすることもできる:
マイクロダイジェスト2 JP PDFをダウンロードまた、AD/PD & CONyからマイクロダイジェストをダウンロードすることもできる:
マイクロダイジェスト1 JP PDFをダウンロード





